1. Đề thi Hóa học lớp 10 học kỳ I số 01
I. Phần trắc nghiệm
Câu hỏi 1: Xem phản ứng hóa học dưới đây:
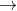
A. 18
B. 19
C. 20
D. 16
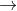
A. 6
B. 8
C. 4
D. 10
Câu 3: Khi cho 11,2 gam Fe tác dụng với HNO3, thu được khí X có thể tích 13,44 lít. Khí X là loại nào?
A. N2
B. NO2
C. NO
D. N2O
Câu 4: Khi cho 9,6 gam Mg phản ứng với H2SO4, thu được 0,1 mol khí X. Khí X là loại nào?
A. S
B. SO2
C. H2S
D. SO3
Câu 5: Khi cho 5,4 gam Al phản ứng với H2SO4 đặc, nóng, thu được 6,72 lít khí X ở điều kiện tiêu chuẩn. Tổng hệ số cân bằng của phản ứng là bao nhiêu?
A. 18
B. 20
C. 11
D. 8
Câu 6: Khi phản ứng Al với HNO3, thu được hỗn hợp khí N2 và NO với tỷ lệ mol 1:1. Tổng hệ số cân bằng của HNO3 là bao nhiêu?
A. 63
B. 104
C. 102
D. 98
Câu 7: Khi Zn phản ứng với HNO3, thu được hỗn hợp khí gồm N2O và NO với tỷ lệ thể tích là 2:3. Tổng hệ số của phản ứng là bao nhiêu?
A. 62
B. 58
C. 64
D. 80
Câu 8: Cho m gam Zn phản ứng với HNO3, thu được 6,72 lít khí N2O. Tính giá trị của m.
A. 16,5
B. 7,8
C. 13,5
D. 26,5
Câu 9: Cho m gam Al phản ứng với H2SO4, thu được 13,44 lít khí H2S. Tính giá trị của m.
A. 32,2
B. 43,2
C. 44,2
D. 65,2
A. Tăng 13,2 gam
B. Giảm 13,2 gam
C. Tăng 19,2 gam
D. Không thay đổi
Câu 11: Khi cho 8,3 gam hỗn hợp Al và Fe phản ứng với HNO3, thu được 13,44 lít khí NO2 ở điều kiện tiêu chuẩn. Xác định tỷ lệ phần trăm của Al trong hỗn hợp.
A. 35,5%
B. 32,53%
C. 67,17%
D. 56,15%
Câu 12: Khi cho 7,8 gam hỗn hợp Al và Mg phản ứng với H2SO4, thu được 8,96 lít khí SO2 ở điều kiện tiêu chuẩn. Tính tỷ lệ khối lượng giữa Al và Mg trong hỗn hợp.
A. 9/3
B. 9/4
C. 27/24
D. 54/19
Câu 13: Khi cho hỗn hợp m gam Al và Cu, với tỷ lệ mol 1:2, phản ứng với HNO3 và thu được 1,568 lít khí N2, hãy xác định giá trị của m.
A. 13,2
B. 15,5
C. 16,8
D. 16,5
Câu 14: Khi cho 5,4 gam Al phản ứng với H2SO4 đặc và thu được 6,72 lít khí X ở điều kiện tiêu chuẩn, tổng hệ số cân bằng của phản ứng là bao nhiêu?
A. 12
B. 18
C. 19
D. 20
II. Phần tự luận
Câu 1: Cân bằng phản ứng
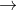
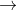
Câu 2: Cho 4,4 gam hỗn hợp hai kim loại thuộc nhóm IIA ở hai chu kỳ liên tiếp vào dung dịch HCl dư, thu được dung dịch X và 3,36 lít khí H2 ở điều kiện tiêu chuẩn
a. Xác định tên hai kim loại và tính phần trăm khối lượng của chúng trong hỗn hợp ban đầu
b. Nếu khối lượng HCl sử dụng là 200 gam, tính nồng độ phần trăm của các muối trong dung dịch X.
Câu 3: Hỗn hợp chứa Al và Mg có tổng khối lượng 3,54 gam được chia thành hai phần bằng nhau:
Phần 1: Tác dụng với HCl dư, thu được 1,904 lít khí H2 ở điều kiện tiêu chuẩn
Phần 2: Hòa tan trong HNO3 loãng dư, thu được hỗn hợp khí NO và N2O với tỷ lệ mol là 1:2
Tính thể tích của các khí NO và N2O ở điều kiện tiêu chuẩn
2. Đề kiểm tra hóa học lớp 10 học kỳ 1, đề số 02
I. Phần trắc nghiệm
Câu 1: Khi hòa tan m gam Al vào dung dịch HNO3 rất loãng, thu được hỗn hợp khí gồm 0,03 mol N2O và 0,01 mol NO. Tính giá trị m:
A. 8,1
B. 13,5
C. 2,43
D. 1,35
Câu 2: Cho 2 gam một kim loại thuộc nhóm IIA phản ứng với dung dịch HCl, tạo ra 5,55 gam muối clorua. Kim loại đó là gì?
A. Be
B. Ba
C. Ca
D. Mg
Câu 3: Cho 3,9 gam K phản ứng với 101,8 gam H2O. Tính nồng độ phần trăm của dung dịch thu được.
A. Kết quả khác
B. 5,3
C. 5,5
D. 4,8
Câu 4: Hòa tan m gam Al vào dung dịch HNO3 loãng, thu được hỗn hợp khí với 0,03 mol N2O và 0,01 mol NO. Tính giá trị m.
A. 8,1
B. 13,5
C. 2,43
D. 1,35
Câu 5: Hòa tan hoàn toàn 2,81 gam hỗn hợp gồm FeSO3, MgO và ZnO vào 550 ml dung dịch H2SO4 0,1M. Sau phản ứng, khối lượng muối khan thu được là bao nhiêu gam?
A. 5,81
B. 6,81
C. 3,81
D. 4,81
Câu 6: Hòa tan 2,16 gam FeO vào dung dịch HNO3 loãng, thu được V lít khí NO duy nhất ở điều kiện tiêu chuẩn. Tính V.
A. 0,224 lít
B. 0,336
C. 0,448
D. 2,240
Câu 7: Một kim loại nặng 2,52 gam phản ứng hoàn toàn với dung dịch H2SO4 loãng và tạo ra 6,84 gam muối sunfat. Kim loại đó là gì?
A. Zn
B. Al
C. Fe
D. Mg
Câu 8: Hỗn hợp X chứa 2,13 gam ba kim loại Mg, Cu và Al dưới dạng bột phản ứng hoàn toàn với oxi tạo ra hỗn hợp Y có khối lượng 3,73 gam. Thể tích dung dịch HCl 2M cần thiết để phản ứng hết với Y là:
A. 20 ml
B. 50 ml
C. 100 ml
D. 90 ml
Câu 9: Tỉ lệ số phần tử HNO3 đóng vai trò là chất oxi hóa và môi trường trong phản ứng:
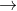
A. 1: 3
B. 1: 10
C. 1: 9
D. 1: 2
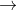
A. chỉ bị oxy hóa
B. chỉ bị khử
C. vừa bị oxy hóa, vừa bị khử
D. không bị oxy hóa, không bị khử
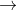
A. SO2 đóng vai trò chất oxi hóa, Cl2 là chất khử
B. SO2 là chất khử, H2O là chất oxi hóa
C. Cl2 đóng vai trò chất oxi hóa, H2O là chất khử
D. Cl2 là chất oxi hóa, SO2 là chất khử
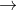
A. 13
B. 14
C. 15
D. 16
3. Đề thi môn Hóa học lớp 10 kỳ 1 số 03
Câu 1: Cân bằng phương trình phản ứng hóa học dưới đây bằng phương pháp cân bằng electron:
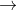
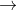
Câu 2: Hoàn thiện sơ đồ phản ứng hóa học sau đây:
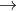
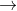
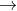
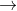
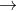
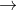
Câu 3. Kim loại A có hóa trị n. Khi hòa tan 1,62 gam A trong HCl dư, thu được 2,016 lít khí H2 ở điều kiện tiêu chuẩn. Kim loại B có hóa trị M. Khi hòa tan 2,24 gam B trong dung dịch HNO3, thu được 896 ml khí NO.
a. Xác định hai kim loại A và B
b. Hỗn hợp X gồm kim loại A và B với khối lượng tổng là 3,61 gam. Cho hỗn hợp X tác dụng với V ml dung dịch H2SO4 0,1M và HCl 0,18M, phản ứng vừa đủ sinh ra 2,128 lít khí H2 ở điều kiện tiêu chuẩn và dung dịch Y. Sau khi cô cạn dung dịch Y, thu được b gam hỗn hợp muối.
- Xác định khối lượng từng kim loại trong hỗn hợp ban đầu
- Tính thể tích dung dịch HCl
- Tính khối lượng b?
Câu 4. Hỗn hợp A chứa Cl và oxi. Khi cho hỗn hợp A phản ứng với 4,8 gam Mg và 8,1 gam Al, thu được 37,05 gam hỗn hợp muối clorua và oxit. Tính phần trăm theo khối lượng và thể tích của Cl2 và O2 trong hỗn hợp A.
>> Xem chi tiết đề kiểm tra hóa học lớp 10 tại đây
