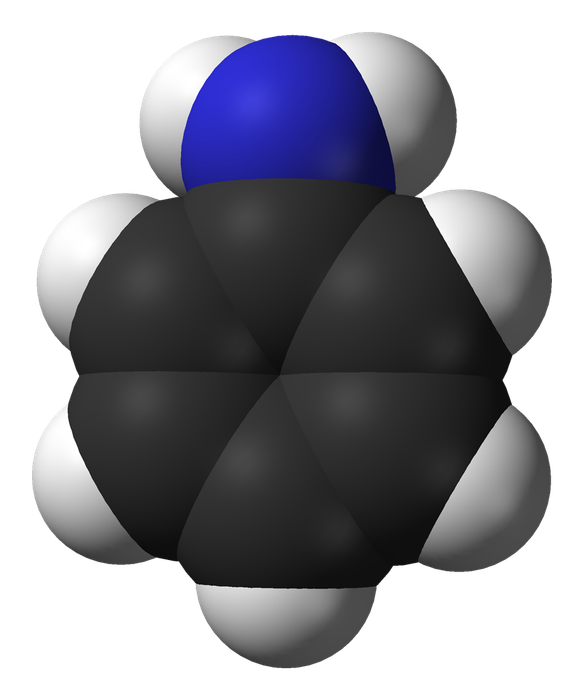
Anilin (bắt nguồn từ từ tiếng Pháp aniline /anilin/), còn được viết là a-ni-lin, hay còn gọi là phenyl amin hoặc amino benzen, là một hợp chất hữu cơ thuộc dãy đồng đẳng amin với công thức phân tử C6H7N. Đây là một trong những amin thơm đơn giản và quan trọng nhất, chủ yếu dùng để sản xuất PU (poly ure). Giống như các amin thơm khác, anilin có mùi khó chịu của cá ươn. Anilin ít tan trong nước (trừ khi đun sôi) và gây bỏng rát khi tiếp xúc với da. Cồn, xăng và dầu ăn dễ dàng hòa tan anilin, vì vậy để xử lý anilin bị đổ, người ta thường dùng cồn hoặc xăng. Anilin cũng là một chất độc có mùi xốc và dễ cháy, tạo ra khói khi cháy.
Cấu trúc
Anilin bao gồm một nhóm phenyl liên kết với một nhóm amin. Anilin có cấu trúc hơi hình tháp, với sự lai hóa của nguyên tử nitơ ở mức độ giữa sp3 và sp2. Kết quả là, cặp electron đơn độc của nitơ nằm trong một orbital lai hóa spx với tính chất p cao. Nhóm amino trong anilin phẳng hơn (có dạng 'hình tháp nông hơn') so với nhóm amino trong amin béo, do sự liên hợp của cặp đơn với nhóm thế aryl. Hình học quan sát được là kết quả của sự thỏa hiệp giữa hai yếu tố cạnh tranh: sự ổn định của cặp e N trong một orbital với nhân vật pyramidalization thấp về năng lượng, và sự xen phủ của cặp đơn lẻ vào vòng aryl tạo ra sự thuần nhất.
Phù hợp với các yếu tố này, các anilin được thay thế bằng các nhóm cho điện tử có hình chóp hơn, trong khi các anilin có nhóm rút điện tử sẽ phẳng hơn. Trong anilin nguyên bản, cặp đơn lẻ có tính chất xấp xỉ 12% s, tương ứng với phép lai sp7.3. (Để so sánh, các ankylamin thường có các cặp đơn lẻ trong các orbital gần với sp3.)
Góc hình chóp giữa liên kết C – N và phân giác của góc H – N – H là 142,5°. (Để so sánh, trong metylamin có hình tháp mạnh hơn, góc này là ~ 125°, trong khi nitơ phẳng của formamit có góc 180°.) Khoảng cách C – N trong anilin cũng ngắn hơn, chỉ 1,41 Å so với 1,47 Å của xyclohexylamin, cho thấy có liên kết π một phần giữa N và C.
Điều chế
Benzen được nitrat hóa bởi hỗn hợp axit nitric và axit sunfuric đậm đặc ở 50-60°C, tạo ra nitrobenzen:
Đây là một trong những quy trình sản xuất nguy hiểm nhất do phản ứng tỏa nhiệt mạnh, có thể gây nổ.
Sau đó, nitrobenzen được chuyển hóa thành anilin:
Các kim loại nhóm 10 như nickel, palladium và platin được sử dụng làm chất xúc tác chính.
Anilin cũng có thể được điều chế từ amoniac và phenol có nguồn gốc từ cumene.
Tính chất
Quá trình oxi hóa
Anilin từ từ bị oxi hóa trong không khí, tạo ra những vệt màu nâu đen.
Đặc tính base
Anilin là một base yếu. Những amin thơm như anilin có tính base kém hơn amoniac. Anilin khó tan trong nước, nhưng nước sôi có thể hòa tan được nó. Dung dịch anilin không làm đổi màu quỳ tím.
Đặc điểm của vòng benzen
Vì phân tử có nhóm -NH2, mật độ electron trong vòng benzen cao hơn so với benzen. Do đó, khi xảy ra phản ứng thế, 2 vị trí ortho và para (so với nhóm -NH2) sẽ được ưu tiên thế, khiến phản ứng diễn ra dễ dàng hơn.
Đặc tính của nhóm amin
Anilin phản ứng với acid nitric ở nhiệt độ thấp (0-5 độ C) tạo ra các hợp chất diazoni.
C6H5NH2 + HONO ⟶ C6H5N2Cl + 2H2O
Các hợp chất diazoni là tiền chất để sản xuất thuốc nhuộm azo. Do đó, một lượng lớn anilin được sản xuất làm nguyên liệu cho các loại thuốc nhuộm khác nhau.
Anilin cũng có thể phản ứng với các alcohol trong phản ứng Friedel-Crafts.
C6H5NH2 + 2CH3OH → C6H5N(CH3)2 + 2H2O
C6H5NH2 + CH3OH → C6H5NHCH3 + H2O
Anilin còn có thể phản ứng trực tiếp với các dẫn xuất halogen để tạo ra các hợp chất amin bậc hai hoặc bậc ba, sau đó dùng NaOH/KOH để tách acid halogen ra khỏi hỗn hợp.
Các ứng dụng
Phần lớn anilin được sử dụng để sản xuất methylenedianilin, đồng thời còn ứng dụng trong sản xuất thuốc nhuộm, chế biến cao su, sản xuất polymer, và dược phẩm.
Một lượng lớn anilin được dùng để sản xuất 4,4′-Methylenedianiline ( MDA ), chất này lại là nguyên liệu cho sản xuất Auramine O.
Các liên kết bên ngoài
- Avogadro savety sheet Lưu trữ ngày 2006-10-04 tại Wayback Machine
- Acros savety sheet
- International Chemical Safety Card 0011
- National Pollutant Inventory - Aniline Lưu trữ ngày 2006-09-10 tại Wayback Machine
- NIOSH Pocket Guide to Chemical Hazards
- IARC Monograph 'Aniline' Lưu trữ ngày 2005-10-12 tại Wayback Machine
- Computational Chemistry Wiki entry Lưu trữ ngày 2007-09-27 tại Wayback Machine
- Aniline electropolymerisation
