| Acid peroxymonosulfuric | |
|---|---|
Skeletal formula of peroxymonosulfuric acid | |
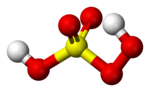
Ball and stick model of peroxymonosulfuric acid | |
| Tên hệ thống | Peroxysulfuric acid, Sulfuroperoxoic acid |
| Tên khác | Peroxosulfuric acid Peroxomonosulfuric acid Persulfuric acid |
| Nhận dạng | |
| Số CAS | 10361-76-9 |
| PubChem | 2754594 |
| Số EINECS | 231-766-6 |
| ChEBI | 29286 |
| Ảnh Jmol-3D | ảnh ảnh 2 |
| SMILES | đầy đủ |
| Tham chiếu Gmelin | 101039 |
| Thuộc tính | |
| Công thức phân tử | H 2SO 5 |
| Khối lượng mol | 114,078 g mol |
| Bề ngoài | Tinh thể trắng |
| Khối lượng riêng | 2,239 g cm |
| Điểm nóng chảy | |
| Điểm sôi | |
| Cấu trúc | |
| Tọa độ | Tứ diện tại S |
| Các nguy hiểm | |
| Nguy hiểm chính | Chất oxy hóa mạnh |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa).
(cái gì ?)
Tham khảo hộp thông tin | |
Axít peroxymonosulfuric, còn được biết đến với các tên khác như axít persulfuric, axít peroxysulfuric hay axít caroic, là một loại axít vô cơ có công thức hóa học H2SO5. Axít này tồn tại dưới dạng lỏng ở nhiệt độ phòng, với cấu trúc trung tâm là lưu huỳnh(VI) hình tứ diện đặc trưng; công thức kết nối là HO-O-S(O)2-OH. Đây là một trong những chất oxy hóa mạnh nhất với điện thế oxy hóa E0 = +2.51 V và có khả năng dễ cháy cao.
H2SO5 thường bị nhầm lẫn với H2S2O8, hợp chất được gọi là axít peroxydisulfuric. Axít disulfuric, có vẻ như được sử dụng rộng rãi hơn nhờ các muối kim loại kiềm của nó, có cấu trúc HO-S(O)2-O-O-S(O)2-OH.
Lịch sử
Axít H2SO5 lần đầu tiên được Heinrich Caro mô tả vào năm 1898 và tên của hợp chất này được đặt theo tên của ông.
Tổng hợp và sản xuất
Để điều chế axít Caro trong phòng thí nghiệm, người ta kết hợp axít chlorrosulfuric với hydro peroxide.
- H2O2 + ClSO2OH ⇌ H2SO5 + HCl
Việc sản xuất axít Caro quy mô lớn thường được thực hiện ngay tại chỗ do tính không ổn định của nó. Theo phát minh của Martin, axít Caro được chế tạo từ axít sulfuric có nồng độ >85% và hydro peroxide có nồng độ <50% ('dung dịch Piranha').
- H2O2 + H2SO4 ⇌ H2SO5 + H2O
Ứng dụng trong ngành công nghiệp
H2SO5 trước đây được dùng để tẩy uế và trong các ứng dụng làm sạch, như xử lý nước hồ bơi và vệ sinh răng giả. Các muối của H2SO5 có triển vọng trong việc khử lignin từ gỗ.
Các muối amoni, natri và kali của H2SO5 được áp dụng trong ngành công nghiệp nhựa như chất xúc tác cho polymer hóa, chất ăn mòn, chất tẩy hồ trong dệt may, cải tạo đất, và trong xử lý màu và mùi của dầu.
Kali peroxymonosulfat, KHSO5, là muối kali của axít peroxymonosulfuric và được sử dụng phổ biến như một tác nhân oxy hóa.
Rủi ro
Acid này có tính chất dễ gây nổ. Đã có các sự cố nổ được ghi nhận tại Đại học Brown và Sun Oil. Giống như các chất oxy hóa mạnh khác, acid peroxysulfuric cần được bảo quản xa các hợp chất hữu cơ như ete và keton để tránh nguy cơ tạo ra các phân tử không ổn định như axeton peroxide.
Hợp chất lưu huỳnh | |
|---|---|
| |
Hợp chất hóa học
|
Hợp chất hydro |
|---|
