Giải bài tập SGK Hóa học 10 Cánh diều Bài 2 trang 11, 12, 13, 14, 15 giúp học sinh tham khảo để trả lời câu hỏi và làm bài tập thảo luận và vận dụng trong sách giáo khoa về Thành phần của nguyên tử.
Lời giải bài 2 Hóa 10 Cánh diều được soạn thảo một cách chi tiết, đầy đủ và chính xác, phù hợp với nội dung sách giáo khoa. Bộ tài liệu giải bài tập Hóa 10 về Thành phần của nguyên tử trong sách Cánh diều là nguồn tư liệu quan trọng giúp hỗ trợ học sinh lớp 10 trong quá trình giải bài tập. Đồng thời, phụ huynh có thể sử dụng để hướng dẫn con em học tập và cải thiện phương pháp giải bài tập phù hợp.
Giải bài tập Hóa học 10 Bài 2: Thành phần của nguyên tử
- Trả lời câu hỏi và thảo luận về Hóa 10 Bài 2 Cánh diều
- Trả lời câu hỏi Luyện tập Hóa học 10 Bài 2
- Giải SGK Hóa 10 bài 2 trang 15
Thảo luận về câu hỏi Hóa học 10 bài 2 Cánh diều
Câu hỏi 1 trang 11
Tất cả các nguyên tử đều có tổng số proton và electron bằng nhau. Dựa vào bảng 2.1, hãy lập luận để chứng minh rằng: số proton và số electron trong một nguyên tử luôn bằng nhau.

Gợi ý cho đáp án
Trong một nguyên tử, giả sử số proton, neutron, electron lần lượt là x, y, z
Do các nguyên tử có tổng điện tích bằng không.
Dựa vào thông tin về điện tích của các hạt trong bảng 2.1.
Ta suy ra: (+1).x + (-1).y + 0.z = 0
Kết quả là: x – y = 0
Do đó, ta có: x = y
Nhận xét: Trong một nguyên tử, số proton và số electron luôn bằng nhau.
Câu 2 ở trang 12
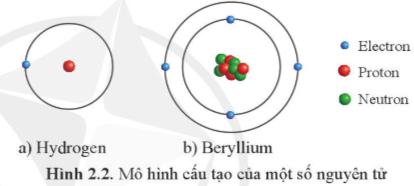
Hãy so sánh sự khác biệt về cấu trúc nguyên tử giữa hydrogen và beryllium dựa trên Hình 2.2.
Giải đáp:
Dựa vào Hình 2.2, chúng ta có thể nhận thấy:
Nguyên tử hydrogen bao gồm: electron và proton
Nguyên tử beryllium bao gồm: electron, proton và neutron
Do đó, nguyên tử hydrogen không chứa hạt neutron, trong khi nguyên tử beryllium có hạt neutron.
Đáp: Trả lời câu hỏi ôn tập Hóa học 10 Bài 2
Câu 1 ở trang 13
Hạt proton và neutron nặng hơn hạt electron bao nhiêu lần?
Đáp: Gợi ý đáp án
Xem xét từ bảng 2.1
+ Khối lượng của electron là 0,00055 amu
+ Khối lượng của proton là 1 amu
+ Khối lượng của neutron là 1 amu
Hạt proton nặng hơn hạt electron bao nhiêu lần:

Hạt neutron nặng hơn hạt electron bao nhiêu lần:

Câu 2 ở trang 13
Hãy chỉ ra số lượng hạt proton cần để có tổng khối lượng bằng 1 gam.
Đề xuất: Gợi ý đáp án
Chuyển đổi 1 amu = 1,6605.10-27 kg = 1,6605.10-24 g
Ta tính được:
1 hạt proton có khối lượng là 1 amu, tương đương với 1,6605.10-24 gam
x hạt proton có khối lượng là x amu, tương đương với 1 gam
Số lượng hạt proton cần để có tổng khối lượng bằng 1 gam là:
x = 1.1 : 1,6605.10-24 ≈ 1,6605.1024 (hạt).
Câu 3 ở trang 13
Khi các nguyên tử tiếp xúc để tạo liên kết hóa học, sự tiếp xúc ban đầu giữa hai nguyên tử sẽ xảy ra ở đâu?
A. Lớp vỏ với lớp vỏ
B. Lớp vỏ với hạt nhân
C. Hạt nhân với hạt nhân
Đề xuất: Gợi ý đáp án
Khi các nguyên tử gần nhau để hình thành liên kết hóa học, sự tiếp xúc đầu tiên giữa hai nguyên tử sẽ diễn ra giữa lớp vỏ và lớp vỏ.
Đáp án A
Trả lời trong sách giáo khoa Hóa học lớp 10, bài 2 trang 15
Bài 1
Một loại nguyên tử hydrogen đơn giản chỉ gồm 1 electron và 1 proton. Câu nào sau đây đúng khi nói về nguyên tử hydrogen này?
(a) Đây là nguyên tử nhẹ nhất trong số tất cả các nguyên tử đã biết đến cho đến nay.
(b) Khối lượng của nguyên tử xấp xỉ 2 amu.
(c) Hạt nhân của nguyên tử có khối lượng lớn gấp khoảng 1818 lần khối lượng của lớp vỏ.
(d) Kích thước của nguyên tử bằng kích thước của hạt nhân.
Đề xuất: Gợi ý đáp án
(a) Đúng vì:
Hydrogen có khối lượng nguyên tử nhỏ nhất là khoảng 1, vì vậy nó là nguyên tử nhẹ nhất được biết đến cho đến nay.
Tuy nhiên, 1 amu không thể chính xác với khối lượng nguyên tử của hydrogen.
(b) Sai vì:
Khối lượng nguyên tử hydrogen = 0,00055. 1 + 1. 1 + 1. 0 ≈ 1amu
(c) Đúng vì:
+ Nguyên tử được tạo thành từ hạt proton và neutron tạo thành hạt nhân, cùng với các hạt electron tạo thành vỏ nguyên tử.
+ Hạt nhân nguyên tử gồm các hạt proton và neutron
=> Khối lượng của hạt nhân nguyên tử lớn gấp nhiều lần so với khối lượng của vỏ nguyên tử.

(d) Sai vì:
So với kích thước của nguyên tử, kích thước của hạt nhân không hề nhỏ.
Kết luận: Các phát biểu đúng là (a) và (c)
Bài 2
Hiện tượng sấm sét được tạo ra bởi các đám mây chứa hạt nước nhỏ mang điện tích. Một thí nghiệm đã chỉ ra rằng một giọt nước có đường kính 50 μm, mang điện tích âm là -3,33. 10-17C. Hỏi, điện tích âm của giọt nước tương đương với bao nhiêu electron?
Gợi ý đáp án
Một electron mang điện tích -1,602.10-19C.
Sử dụng công thức tính toán.
Số electron tương đương với điện tích âm của giọt nước là:

Bài 3
Nguyên tử trở nên trung hòa về điện do
A. được tạo thành từ các hạt không mang điện.
B. tổng số proton bằng tổng số electron.
C. tổng số electron bằng tổng số neutron.
D. tổng số hạt neutron bằng tổng số hạt proton.
Gợi ý đáp án
Nguyên tử trở nên trung hòa về điện do có tổng số proton bằng tổng số electron.
Đáp án B
Bài 4
Trả lời các câu hỏi sau:
a) Hạt nào tồn tại trong hạt nhân của nguyên tử?
b) Hạt nào tồn tại ở vỏ của nguyên tử?
c) Loại hạt nào mang điện trong nguyên tử?
d) Kích thước của nguyên tử lớn hơn kích thước của hạt nhân khoảng bao nhiêu lần?
Gợi ý đáp án
a) Trong hạt nhân nguyên tử, có sự tồn tại của proton và neutron.
b) Ở lớp vỏ nguyên tử, chúng ta tìm thấy electron.
c) Loại hạt mang điện trong nguyên tử là:
Electron (có điện tích âm -1)
Proton (có điện tích +1)
d) Kích thước của nguyên tử lớn hơn kích thước của hạt nhân từ 104 đến 105 lần.
Kích thước của hạt nhân nhỏ hơn kích thước của nguyên tử từ 10-5 đến 10-4 lần.
Bài 5
Tính tổng số electron, proton và neutron trong một phân tử nước (H2O). Biết rằng trong mỗi phân tử nước, mỗi nguyên tử hydrogen đóng góp 1 proton và 1 electron; còn nguyên tử oxygen đóng góp 8 neutron và 8 proton.
Gợi ý đáp án
Trong một nguyên tử, số proton luôn bằng số electron.
=> Số proton = Số electron = 8
=> Hydrogen có 1 proton, 1 electron và Oxygen có 8 proton, 8 electron, 8 neutron.
1 phân tử nước (H2O) bao gồm 2 nguyên tử hydrogen và 1 nguyên tử oxygen.
Do đó, tổng số hạt trong 1 phân tử nước là:
2 .(1 + 1) + 1. (8 + 8 + 8) = 28 hạt
