1. Bộ 30 đề thi học sinh giỏi Hóa học lớp 9 có lợi ích gì?
Bộ 30 đề thi giỏi Hóa học lớp 9 mang đến những lợi ích sau:
- Bộ đề này cung cấp một tập hợp các bài thi giúp học sinh luyện tập và giải quyết các vấn đề liên quan đến môn Hóa học. Việc làm các đề thi này giúp củng cố và ôn tập kiến thức đã học trong lớp 9.
- Tài liệu này là công cụ hỗ trợ đắc lực cho học sinh chuẩn bị cho kỳ thi học sinh giỏi môn Hóa học. Các đề thi trong bộ sưu tập này giúp học sinh làm quen với dạng câu hỏi thường gặp trong các kỳ thi thực tế.
- Đề thi môn Hóa học thường yêu cầu học sinh phải vận dụng tư duy logic và giải quyết các vấn đề phức tạp. Giải các đề thi trong bộ này sẽ giúp học sinh nâng cao kỹ năng giải quyết vấn đề của mình.
- Thực hành với các đề thi khó trong bộ sưu tập này có thể giúp học sinh gia tăng sự tự tin và kiên nhẫn khi đối mặt với các thử thách học tập.
- Làm quen với các đề thi trong bộ sưu tập này giúp học sinh hình thành thói quen ôn tập liên tục, đặc biệt khi chuẩn bị cho các kỳ thi quan trọng.
Tóm lại, bộ 30 đề thi học sinh giỏi môn Hóa học lớp 9 hỗ trợ học sinh trong việc ôn tập, phát triển kỹ năng giải quyết vấn đề, chuẩn bị cho kỳ thi học sinh giỏi và tăng cường sự tự tin trong môn Hóa học.
2. Bộ 30 đề thi học sinh giỏi môn Hóa học lớp 9 chọn lọc
ĐỀ THI HỌC SINH GIỎI HÓA HỌC 9 - ĐỀ SỐ 1
Câu 1: (6 điểm)
1 - Tính tổng số proton, neutron và electron trong hai nguyên tử của nguyên tố A và B là 78. Trong đó, số hạt mang điện vượt số hạt không mang điện là 26. Số hạt mang điện của nguyên tố A nhiều hơn B là 28. Xác định nguyên tố A và B?
Các nguyên tố có điện tích hạt nhân: ZN = 7 ; ZNa = 11 ; ZCa = 20 ; ZFe = 26 ; ZCu = 29 ; ZC = 6 ; ZS = 16.
2 - Hợp chất của nguyên tố A và D khi hòa tan trong nước tạo ra dung dịch có tính kiềm. Ngược lại, hợp chất của B và D khi hòa tan trong nước tạo ra dung dịch E có tính axit nhẹ. Các hợp chất A, B và D không tan trong nước nhưng tan trong dung dịch E. Xác định các hợp chất được tạo ra từ A và D, B và D, cũng như A, B và D. Viết phương trình phản ứng tương ứng.
3 - Một số nguyên nhân dẫn đến sự hình thành canxicacbonat trong thạch nhũ ở các hang động đá vôi có thể là do canxihiđrocacbonat có các đặc điểm sau:
a. Là chất kết tinh và có khả năng sinh bọt khí.
b. Có thể tan trong nước và không ổn định.
c. Dễ bay hơi và có thể bị rửa trôi.
d. Chất kết tinh và không hòa tan trong nước.
Câu 2: (4 điểm)
1 - Xác định các chất A, B, C, D, E (hợp chất của Cu) trong sơ đồ được cung cấp và viết phương trình hóa học cho từng trường hợp.
2 - Sử dụng nước để nhận diện 4 chất rắn: Na2O, Al2O3, Fe2O3 và Al trong các lọ riêng biệt. Viết các phương trình phản ứng tương ứng.
Câu 3: (4 điểm)
Khi cho 27,4 g Ba vào 400 g dung dịch CuSO4 3,2%, ta thu được khí A, kết tủa B và dung dịch C.
a. Tính thể tích khí A ở điều kiện tiêu chuẩn (đktc).
b. Nung kết tủa B đến khi khối lượng không thay đổi, sẽ thu được bao nhiêu gam chất rắn?
c. Tính nồng độ phần trăm của chất tan có trong dung dịch C.
Câu 4: (6 điểm)
Hỗn hợp A bao gồm rượu etylic và hai axit hữu cơ liên tiếp có cấu trúc CnH2n+1COOH và Cn+1H2n+3COOH. Khi cho 1/2 hỗn hợp A phản ứng hoàn toàn với Na, lượng khí H2 thu được là 3,92 lít (đktc). Đốt cháy 1/2 hỗn hợp A, sản phẩm cháy được hấp thụ hoàn toàn vào dung dịch Ba(OH)2 dư, tạo ra 147,75 g kết tủa và làm tăng khối lượng dung dịch Ba(OH)2 thêm 50,1 g.
a. Xác định công thức hóa học của hai axit trong hỗn hợp.
b. Tính toán thành phần cụ thể của hỗn hợp A.
ĐỀ THI HỌC SINH GIỎI HÓA HỌC 9 - ĐỀ 2
Câu 1. (3 điểm)
Hoàn thành sơ đồ bằng cách viết các phương trình hóa học phù hợp:
Al → Al2O3 → Al(NO3)3 → Al(OH)3 → Na[Al(OH)4] → Al(OH)3 → Al2O3 → Na[Al(OH)4] → Al2(SO4)3 → KAl(SO4)2.12H2O
Câu 2. (4 điểm)
(1) Sử dụng phương pháp hóa học để tách riêng từng chất trong hỗn hợp CuO, Al2O3, SiO2.
(2) Có 5 lọ chứa 5 dung dịch không ghi nhãn gồm: Na2CO3, BaCl2, MgCl2, H2SO4. Không được sử dụng thêm hóa chất nào khác, hãy nhận biết các dung dịch này bằng phương pháp hóa học.
Câu 3. (4 điểm)
Xem hình vẽ dưới đây:
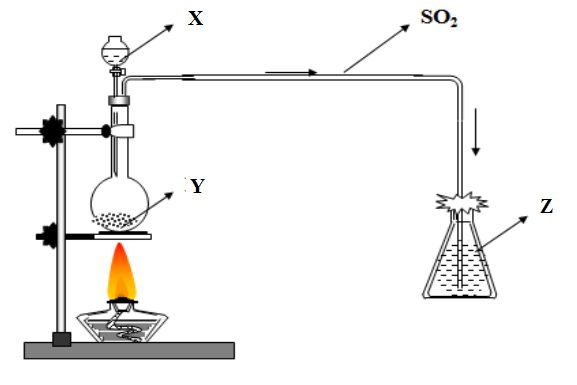
Hình vẽ minh họa thí nghiệm điều chế và kiểm tra tính khử của khí nào trong phòng thí nghiệm?
Xác định các chất X, Y, Z xuất hiện trong thí nghiệm trên.
Giải thích tại sao cần dùng bông tẩm NaOH ở miệng bình thu khí trong thí nghiệm?
(4) Có thể thay thế NaOH bằng dung dịch Ca(OH)2 hoặc H2SO4 không?
(5) Trình bày các tính chất hóa học của khí được điều chế trong hình vẽ trên?
(6) Viết toàn bộ các phương trình hóa học thể hiện thí nghiệm đã mô tả?
Câu 4. (4 điểm)
Có năm chất lỏng A, B, C, D, E. Trong số đó, chất nào là benzen, ancol etylic, axit axetic, dung dịch glucozơ, và nước? Dựa vào các thí nghiệm dưới đây:
- Khi cho tác dụng với Na, các chất A, B, C, D sinh ra khí; còn E không phản ứng.
- Khi tác dụng với CaCO3, các chất A, B, C, E không có phản ứng; trong khi D sinh ra khí.
- Khi cho tác dụng với dung dịch AgNO3/NH3, bạc không xuất hiện trong các chất A, C, D, E; chỉ có B xuất hiện bạc.
- Khi đốt trong không khí, các chất A và E cháy dễ dàng; D cháy được; còn B và C không cháy.
Xác định các chất A, B, C, D, E và viết các phương trình hóa học dựa trên kết quả của các thí nghiệm đã nêu.
Câu 5. (5 điểm)
Khi hòa tan hoàn toàn 5,68 gam hỗn hợp A gồm MgCO3 và CaCO3 vào dung dịch HCl dư, khí CO2 sinh ra được hấp thụ hoàn toàn bởi 225 ml dung dịch Ba(OH)2 0,2M, tạo ra 5,91 gam kết tủa. Tính số mol của từng chất trong hỗn hợp A.
Một lượng chất hữu cơ X khi đốt cháy hoàn toàn cần 6,72 lít O2 (đktc). Toàn bộ sản phẩm cháy chỉ tạo ra CO2 và H2O, khi cho vào nước vôi trong thu được 10 gam kết tủa và 200 ml dung dịch muối có nồng độ 0,5M, dung dịch này nặng hơn nước vôi ban đầu là 8,6 gam. Xác định công thức đơn giản nhất của X.
3. “Bí kíp” ôn luyện thi học sinh giỏi hóa lớp 9
Dưới đây là một số bí quyết ôn luyện hiệu quả để đạt thành tích cao trong kỳ thi học sinh giỏi môn Hóa học lớp 9:
- Xác định rõ mục tiêu học tập và lập kế hoạch cụ thể. Phân chia thời gian ôn luyện theo ngày, tuần và tháng để đảm bảo bao quát toàn bộ kiến thức.
- Nắm vững chương trình học lớp 9 là rất quan trọng. Học theo chương trình giúp bạn không bỏ sót bất kỳ kiến thức quan trọng nào.
- Sách giáo trình là nguồn tài liệu chính thức và tin cậy. Đảm bảo bạn hiểu và thực hành các bài tập trong sách giáo trình.
- Tạo một sổ tay Hóa học để ghi chép các kiến thức quan trọng, công thức và ví dụ. Việc ghi chép tay giúp bạn ghi nhớ lâu hơn.
- Bên cạnh sách giáo trình, hãy tìm kiếm thêm tài liệu bổ trợ như sách tham khảo, đề thi mẫu, và tài liệu trực tuyến để tăng cường ôn luyện.
- Hóa học yêu cầu thực hành nhiều. Thực hiện nhiều bài tập và ví dụ để nâng cao kỹ năng giải quyết các dạng bài tập khác nhau.
- Nếu có cơ hội, tham gia các khóa học hoặc lớp học thêm về Hóa học để mở rộng kiến thức và trao đổi với giáo viên cũng như bạn học.
- Giải nhiều đề thi mẫu Hóa học để quen với định dạng và kiểu câu hỏi trong kỳ thi. Điều này giúp bạn cải thiện tốc độ và tự tin hơn.
- Thường xuyên làm bài thi thử để đánh giá khả năng của bạn. Sau mỗi lần thi, phân tích kết quả và tập trung vào các điểm yếu để cải thiện.
- Vào tuần hoặc tháng trước kỳ thi, hãy lập kế hoạch ôn tập theo mức độ ưu tiên của từng chủ đề.
- Đảm bảo có giấc ngủ đầy đủ, chế độ ăn uống cân bằng và duy trì sức khỏe tốt. Sức khỏe tốt giúp bạn tập trung và làm việc hiệu quả hơn.
- Trong kỳ thi, nếu gặp câu hỏi khó, hãy làm các câu hỏi dễ trước, rồi quay lại giải quyết các câu hỏi khó hơn.
- Tự tin là chìa khóa để vượt qua áp lực thi cử. Tin vào khả năng của bạn và nỗ lực hết sức trong từng bài thi.
Nhớ rằng ôn luyện là một hành trình dài, cần sự kiên nhẫn và nỗ lực liên tục. Chúc bạn thành công trong kỳ thi học sinh giỏi môn Hóa học!
Dưới đây là toàn bộ thông tin từ bài viết của Mytour về 'Tuyển tập 30 đề thi học sinh giỏi Hóa học - lớp 9'. Chúng tôi xin chân thành cảm ơn quý bạn đọc đã dành thời gian theo dõi bài viết này!
