
Bốc hơi hay bay hơi là quá trình chất lỏng chuyển hóa thành hơi trên bề mặt chất lỏng. Đun sôi là một dạng khác của quá trình hóa hơi, xảy ra đồng đều trong toàn bộ khối lượng chất lỏng.
Thông thường, các phân tử trong nước không có đủ năng lượng để rời khỏi chất lỏng. Tuy nhiên, khi nhiệt độ tăng đủ, chất lỏng sẽ nhanh chóng chuyển thành hơi (xem điểm sôi). Các phân tử va chạm và trao đổi năng lượng ở nhiều mức độ khác nhau, tùy thuộc vào cách chúng va chạm. Đôi khi, sự chuyển hóa này chỉ xảy ra với các phân tử gần bề mặt, tích tụ đủ năng lượng để bay hơi.
Bốc hơi đóng vai trò quan trọng trong chu trình nước. Ánh sáng mặt trời làm nước từ đại dương, hồ và đất bay hơi, cùng với độ ẩm từ các nguồn khác. Trong thủy văn học, bốc hơi và thoát hơi nước (hơi nước từ lỗ khí thực vật) được gọi chung là sự thoát-bốc hơi nước. Bốc hơi chỉ xảy ra khi bề mặt nước tiếp xúc với không khí, cho phép các phân tử chuyển thành hơi nước và tạo ra mây.
Nguyên lý cơ bản
Để các phân tử trong một chất lỏng có thể bay hơi, chúng cần phải gần bề mặt, di chuyển theo hướng thích hợp và có đủ động năng để vượt qua các lực liên kết phân tử trong trạng thái lỏng. Khi chỉ một số ít phân tử đáp ứng được điều kiện này, tốc độ bay hơi sẽ giảm. Vì động năng của một phân tử tỷ lệ với nhiệt độ của nó, sự bay hơi sẽ xảy ra nhanh hơn khi nhiệt độ cao. Khi các phân tử thoát ra nhanh hơn, những phân tử còn lại có động năng trung bình thấp hơn, làm giảm nhiệt độ của chất lỏng. Hiện tượng này còn gọi là sự bay hơi để làm mát. Đây là lý do tại sao việc làm bay hơi mồ hôi giúp làm mát cơ thể. Sự bay hơi cũng xảy ra nhanh hơn khi có lưu lượng lớn hơn giữa pha khí và pha lỏng, và trong các chất lỏng có áp suất hơi cao hơn. Ví dụ, khi giặt ủi, quần áo khô nhanh hơn vào những ngày có gió so với những ngày không có gió. Ba yếu tố chính của sự bay hơi bao gồm nhiệt độ, áp suất khí quyển (xác định độ ẩm) và chuyển động của không khí.
Ở cấp độ phân tử, không có ranh giới rõ ràng giữa trạng thái lỏng và hơi. Thay vào đó, có một lớp Knudsen, nơi mà các pha không xác định. Vì lớp này chỉ dày vài phân tử, còn ở cấp độ vĩ mô thì bề mặt chuyển pha có thể quan sát rõ ràng.
Đối với những chất lỏng không bay hơi ở nhiệt độ và điều kiện nhất định (chẳng hạn như dầu ăn ở nhiệt độ phòng) là vì các phân tử của chúng không có xu hướng chuyển giao năng lượng theo cách bình thường. Do đó, không thể thường xuyên cung cấp năng lượng nhiệt cần thiết cho một phân tử để nó hóa hơi. Tuy nhiên, những chất lỏng này vẫn tiếp tục bay hơi, chỉ là quá trình này diễn ra rất chậm và không dễ dàng quan sát.
Quá trình cân bằng bay hơi
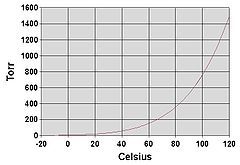
Khi bay hơi xảy ra trong một hệ kín, các phân tử sẽ biến thành hơi trên bề mặt chất lỏng. Phần lớn các phân tử này quay trở lại chất lỏng do khối lượng riêng và áp suất hơi tăng lên. Khi quá trình 'bay hơi và quay trở lại' đạt trạng thái cân bằng, hơi được gọi là 'bão hòa', và không có sự thay đổi về khối lượng riêng, áp suất hơi hoặc nhiệt độ chất lỏng. Đối với hệ thống bao gồm cả hơi và lỏng của một chất tinh khiết, trạng thái cân bằng này liên quan trực tiếp đến áp suất hơi của chất đó, như được mô tả bởi các mối quan hệ Clausius-Clapeyron.
với P1 và P2 là áp suất hơi ở các nhiệt độ T1 và T2 tương ứng, ΔHvap là entanpy bay hơi, và R là hằng số khí. Tốc độ bay hơi trong một hệ mở liên quan đến áp suất hơi trong một hệ kín. Nếu chất lỏng được đun nóng, khi áp suất hơi đạt mức áp suất môi trường xung quanh, chất lỏng sẽ bắt đầu sôi.
Khả năng của một phân tử chất lỏng để bay hơi chủ yếu phụ thuộc vào động năng mà nó có thể đạt được. Ngay cả khi nhiệt độ thấp, nếu phân tử có đủ động năng vượt qua ngưỡng cần thiết, nó vẫn có thể bay hơi.
Các yếu tố ảnh hưởng đến tốc độ bay hơi
- Nồng độ của các chất bay hơi trong không khí
- Khi không khí đã chứa một lượng lớn chất bay hơi, tốc độ bay hơi của chất đó sẽ giảm.
- Nồng độ các chất khác trong không khí
- Nếu không khí đã bão hòa với các chất khác, khả năng tiếp nhận thêm chất bay hơi sẽ giảm đi.
- Lưu lượng không khí
- Yếu tố này liên quan đến các nồng độ đã đề cập. Khi có dòng khí sạch liên tục di chuyển qua một chất, nồng độ của chất đó trong dòng khí sẽ ít có khả năng tăng lên theo thời gian, dẫn đến việc chất đó bay hơi nhanh hơn. Điều này xảy ra do việc giảm lớp ranh giới tại bề mặt bay hơi nhờ vào tốc độ dòng chảy, và giảm khoảng cách khuếch tán trong lớp cố định.
- Lực liên kết phân tử
- Khi các phân tử trong trạng thái lỏng được giữ chặt bởi các lực liên kết mạnh, thì cần nhiều năng lượng hơn để các phân tử có thể thoát ra khỏi bề mặt chất lỏng. Điều này được thể hiện qua entanpy bay hơi của chất đó.
- Áp suất
- Quá trình bay hơi diễn ra nhanh hơn khi lực giữ các phân tử trên bề mặt ít.
- Diện tích bề mặt
- Chất có diện tích bề mặt lớn hơn sẽ bay hơi nhanh hơn nhờ vào số lượng phân tử bề mặt nhiều hơn có khả năng thoát đi.
- Nhiệt độ của chất
- Chất với nhiệt độ cao hơn sẽ làm cho các phân tử có động năng trung bình cao hơn, dẫn đến tốc độ bay hơi nhanh hơn.
- Khối lượng riêng
- Chất lỏng với khối lượng riêng cao hơn sẽ có tốc độ bay hơi chậm hơn.
Sự hấp thụ nhiệt
Quá trình bay hơi liên quan đến việc hấp thụ nhiệt từ môi trường xung quanh.
Ứng dụng
- Trong ngành công nghiệp, sự bay hơi được áp dụng rộng rãi trong các quy trình như in ấn và sơn phủ; thu hồi muối từ dung dịch và làm khô nhiều loại vật liệu như gỗ, giấy, vải và hóa chất.
- Quá trình phơi quần áo diễn ra ngay cả khi nhiệt độ môi trường thấp hơn điểm sôi của nước nhờ vào các yếu tố như độ ẩm thấp, nhiệt năng từ ánh nắng mặt trời và gió. Máy sấy quần áo sử dụng không khí nóng để tăng tốc độ bay hơi của nước.
- Matki / Matka là một loại bình làm bằng đất sét xốp ở Ấn Độ, được sử dụng để lưu trữ và làm mát nước cùng các chất lỏng khác, tương tự như botijo ở Tây Ban Nha.
- Các hệ thống bay hơi làm mát có thể làm giảm nhiệt độ trong một tòa nhà bằng cách thổi không khí khô qua bộ lọc nước.
Quá trình đốt trong khi bay hơi
Khi các giọt nhiên liệu nhận nhiệt và trộn lẫn với khí nóng trong buồng đốt, chúng sẽ bay hơi. Nhiệt (năng lượng) có thể đến từ bức xạ từ các bức tường chịu nhiệt của buồng đốt.
Quá trình đốt trước khi bay hơi
Quá trình cracking xúc tác chuyển đổi các hydro-carbon chuỗi dài thành các phân tử ngắn hơn, nhằm tối ưu hóa hiệu suất hoạt động và giảm khí thải độc hại. Khi hơi nhiên liệu được trộn với không khí theo tỷ lệ tối ưu, hỗn hợp khí và nhiên liệu chuẩn để đốt cháy xăng là 15 phần khí với 1 phần xăng, tương đương với tỷ lệ thể tích 8000/1.
Sự lắng đọng thành màng mỏng
Bài viết chính: Sự bay hơi (lắng đọng) Màng mỏng của vật liệu có thể được hình thành bằng cách làm bay hơi chất và ngưng tụ chúng lên một bề mặt.
Đọc thêm
- Sze, Simon Min. Các thiết bị bán dẫn: Vật lý và Công nghệ. ISBN 0-471-33372-7. Cung cấp một thảo luận chi tiết về việc lắng đọng màng qua quá trình bay hơi.
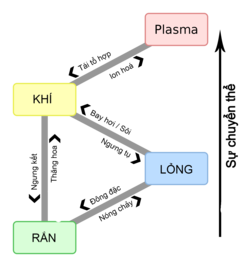
Trạng thái vật chất | ||
|---|---|---|
| Trạng thái |
| |
| Năng lượng thấp |
| |
| Năng lượng cao |
| |
| Các trạng thái khác |
| |
| Chuyển pha |
| |
| Đại lượng |
| |
| Khái niệm |
| |
| Danh sách |
| |
