1. Phương trình hóa học:
C6H5OH + NaOH → C6H5ONa + H2O
2. Hiện tượng phản ứng xảy ra
- Phenol hầu như không tan trong nước lạnh nhưng dễ hòa tan trong dung dịch NaOH
3. Cách thực hiện phản ứng giữa C6H5OH và NaOH
Cho 2ml dung dịch NaOH đặc vào ống nghiệm, sau đó thêm một ít phenol
4. Điều kiện để phản ứng xảy ra
- Phản ứng xảy ra ở điều kiện thường
5. Tìm hiểu thêm về Natri Phenolat
* Tính chất vật lý:
- Hình thức: Chất rắn màu trắng; dễ hòa tan trong nước, rượu và axeton.
- Khối lượng phân tử: 116,9 g/mol
- Không dễ cháy nhưng có thể gây hại và ăn mòn
- Nhiệt độ nóng chảy: 384 độ C
* Tính chất hóa học:
- Tính bazơ mạnh trung bình, có khả năng phản ứng với axit để tạo ra phenol
- Tương tác với các tác nhân alkyl để tạo thành ete alkyl phenyl
- Tham gia tổng hợp ether Williamson với tác nhân axyl hóa, sản phẩm tạo thành là phenyl este
- Natri phenolat là chất dễ bị tác động bởi một số chất thay thế thơm trong quá trình điện di.
6. Bài tập áp dụng liên quan
Bài 1: Xác định phát biểu nào dưới đây là sai?
A. Dung dịch natri phenolat phản ứng với khí CO2, kết tủa tạo ra có thể hòa tan lại trong dung dịch NaOH để thu được natri phenolat.
B. Khi cho phenol phản ứng với dung dịch NaOH, muối tạo thành nếu phản ứng với dung dịch HCl sẽ thu được phenol.
C. Khi axit axetic phản ứng với dung dịch NaOH, muối tạo thành nếu tiếp xúc với khí CO2 sẽ thu được axit axetic trở lại.
D. Khi anilin phản ứng với dung dịch HCl, muối tạo thành nếu phản ứng với NaOH sẽ cho anilin trở lại.
Đáp án: Chọn C. Phát biểu axit axetic phản ứng với dung dịch NaOH, muối tạo ra khi tiếp xúc với khí CO2 sẽ thu được axit axetic trở lại. Axit axetic mạnh hơn H2CO3, nên CO2 không thể phản ứng với muối axetat để tạo axit axetic.
Bài 2: Viết phương trình hóa học cho phản ứng xảy ra và giải thích. Biết rằng có dung dịch vẩn đục khi sục khí CO2 vào dung dịch natri phenolat và có chứa NaHCO3. Nhận xét về tính axit của phenol.
Hướng dẫn giải chi tiết:
Phương trình phản ứng khi sục khí CO2 vào dung dịch phenolat không chứa NaHCO3 như sau:
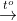
- Khi C6H5OH kết tủa, dung dịch bị vẩn đục do phản ứng tạo ra phenol.
- Nhận xét về tính axit của phenol: Phenol có tính axit yếu hơn so với nấc đầu của axit cacbonic H2CO3, do đó bị axit cacbonic đẩy ra khỏi dung dịch muối.
Bài 3: Thực hiện thí nghiệm bằng cách cho một ít nước vào ống nghiệm chứa mẫu phenol và lắc nhẹ. Mẫu phenol hầu như không thay đổi. Thêm vài giọt dung dịch natri hidroxit, lắc nhẹ, mẫu phenol tan dần. Sục khí cacbonic vào dung dịch vẩn đục. Giải thích các hiện tượng quan sát được.
Lời giải:
- Mẫu phenol gần như không thay đổi vì phenol ít tan trong nước ở điều kiện bình thường.
- Khi thêm dung dịch natri hidroxit, phenol tan do phản ứng với natri hidroxit tạo thành muối natri phenolat tan trong nước:
C6H5OH + NaOH → C6H5ONa + H2O
- Khi sục khí cacbon vào dung dịch, hiện tượng vẩn đục xảy ra do phản ứng sau:
C6H5ONa + CO2 + H2O → C6H5OH kết tủa + NaHCO3
Phenol là một axit rất yếu, bị axit cacbonic đẩy ra khỏi dung dịch muối.
Bài 4: Khi cho phenol vào dung dịch NaOH, phenol tan. Khi sục khí CO2 vào dung dịch, phenol lại tách ra. Giải thích hiện tượng này.
A. Vì phenol là axit rất yếu, yếu hơn cả axit cacbonic.
B. Vì phenol là chất có tính bazơ mạnh.
C. Do phenol là axit mạnh
D. Do phenol là một loại ancol đặc biệt
Bài 5: Có bao nhiêu đồng phân của C8H10O là dẫn xuất của benzen có thể phản ứng với dung dịch NaOH để tạo thành muối và nước? Viết công thức cấu tạo và tên gọi của chúng.
Lời giải:
Dẫn xuất benzen có một nguyên tử oxy khi phản ứng với dung dịch NaOH phải là phenol. Các đồng phân của phenol có công thức phân tử C8H10O.
C2H5C6H4OH (có 3 đồng phân)
(CH3)2C6H3OH (có 6 đồng phân)
Bài 6: Thêm từ từ dung dịch axit nitric vào dung dịch phenol đã bão hòa trong nước và khuấy đều, ta sẽ thấy sự xuất hiện kết tủa màu vàng X với công thức phân tử C6H3N3O7.
a, Giải thích hiện tượng quan sát được trong thí nghiệm bằng các phương trình hóa học.
b, Tính khối lượng kết tủa X thu được khi cho 23,5 gam phenol phản ứng với lượng axit nitric vừa đủ, giả sử phản ứng xảy ra hoàn toàn.
Lời giải:
a, Dựa vào công thức phân tử, ta thấy X có 3 nhóm NO2 thay thế cho 3 nguyên tử hydro trong vòng benzen, phản ứng xảy ra như sau:
C6H5OH + 3HNO3 → (O2N)3C6H2OH kết tủa + 3H2O
b, nphenol = 0,25 mol
Số mol X sinh ra tương ứng với số mol phenol phản ứng, tức là 0,25 mol.
Khối lượng X thu được là mX = 0,25 × 229 = 57,25 (gam)
Bài 6: Kết luận nào sau đây là chính xác?
A. Ancol và phenol đều phản ứng với natri và dung dịch NaOH.
B. Phenol phản ứng với dung dịch NaOH và dung dịch natri cacbonat.
C. Chỉ có ancol mới phản ứng với natri.
D. Chỉ phenol mới phản ứng với dung dịch NaOH.
Bài 7: Hỗn hợp X gồm phenol và ancol etylic. Khi cho 14 gam hỗn hợp tác dụng với natri dư, thu được 2,24 lít khí ở điều kiện tiêu chuẩn.
a. Tính phần trăm khối lượng của các chất trong hỗn hợp X.
b. Nếu 14 gam X phản ứng với dung dịch brom, thì lượng kết tủa của 2, 4, 6 - tribromphenol là bao nhiêu gam? Các phản ứng xảy ra hoàn toàn.
Đáp án:
a. Phần trăm khối lượng của phenol trong hỗn hợp X là 67,14%.
Phần trăm khối lượng của ancol trong hỗn hợp X là 32,86%.
b. Khối lượng kết tủa là 0,1 x 331 = 33,1 gam.
Bài 8: Benzen không phản ứng với dung dịch brom, nhưng phenol làm mất màu nâu đỏ của dung dịch brom rất nhanh. Nguyên nhân là gì?
A. Vì phenol có tính axit.
B. Tính axit của phenol yếu hơn cả axit carbonic.
C. Phenol là dung môi hữu cơ phân cực hơn benzen.
D. Nhờ nhóm -OH, các vị trí ortho và para trong phenol trở nên có điện tích âm cao hơn, tạo điều kiện để tác nhân Br- tấn công nhanh chóng.
Đáp án: Chọn D. Benzen không phản ứng với dung dịch brom, trong khi phenol làm mất màu nâu đỏ của dung dịch brom nhanh chóng do ảnh hưởng của nhóm -OH, khiến các vị trí ortho và para trong phenol có điện tích âm cao, tạo điều kiện thuận lợi cho tác nhân Br- tấn công.
Bài 9: Viết các phương trình hóa học cho các phản ứng xảy ra trong thí nghiệm sau:
a. Đun nóng benzyl clorua trong dung dịch natri hydroxide loãng.
B. Đun nóng hỗn hợp brom benzen và natri hydroxide đặc, dư trong nồi kín. Sau khi phản ứng hoàn tất, axit hóa dung dịch bằng axit clohydric và làm lạnh để thu kết tủa.
C. Dẫn hơi ancol propyl qua ống chứa bột đồng oxit nung nóng, quan sát màu đen của đồng oxit chuyển thành màu đỏ của đồng kim loại và thu được chất lỏng có phản ứng tráng gương.
D. Đun sôi hỗn hợp butan-1-ol với axit sulfuric đặc ở khoảng 180 độ C, sau đó dẫn khí sinh ra qua nước brom.
Bài 9: Phương pháp chế tạo ancol etylic nào sau đây chỉ được thực hiện trong phòng thí nghiệm?
A. Phương pháp lên men tinh bột.
B. Phương pháp thủy phân etyl bromua trong dung dịch kiềm khi đun nóng.
C. Phương pháp hydrat hóa etilen xúc tác bằng axit.
D. Phản ứng khử andehit axetic bằng H2 với xúc tác Ni và đun nóng.
Bài 10: Cho 6,04 gam hỗn hợp X gồm phenol và ancol etylic phản ứng với Na dư, thu được 1,12 lít H2 ở điều kiện tiêu chuẩn. Tính khối lượng kết tủa thu được khi hỗn hợp X tác dụng với dung dịch Br2 dư.
A. Kết tủa thu được là 11,585 gam.
B. Kết tủa thu được là 6,62 gam.
C. Kết tủa thu được là 9,93 gam.
D. Kết tủa thu được là 13,24 gam.
Đáp án: Chọn C. Kết tủa thu được là 9,93 gam.
Bài 11: Một hỗn hợp gồm 25 gam phenol và benzen khi phản ứng với dung dịch NaOH dư tạo ra hai lớp chất lỏng phân cách. Lớp chất lỏng trên có thể tích 19,5 ml và khối lượng riêng 0,8 gam/ml. Hãy xác định khối lượng phenol trong hỗn hợp ban đầu.
A. Khối lượng phenol là 9,4 gam.
B. Khối lượng phenol là 0,625 gam.
C. Khối lượng phenol là 24,375 gam.
D. Khối lượng phenol là 15,6 gam.
Hướng dẫn giải chi tiết: Chọn A. Khối lượng phenol ban đầu là 9,4 gam.
C6H5OH + NaOH → C6H5ONa (tan) + H2O
Lớp chất lỏng tan nằm ở trên do khối lượng riêng lớn, lớp chất lỏng phía trên chính là benzen không tan → mC6H6 = d x V = 19,5 x 0,8 = 15,6 gam
→ mC6H5OH = 25 - 15,6 = 9,4 gam
Bài 12: Cho 15,8 gam hỗn hợp gồm CH3OH và C6H5OH phản ứng với dung dịch brom dư, làm mất màu 48 gam Br2. Khi đốt cháy hoàn toàn hỗn hợp, thể tích CO2 thu được ở điều kiện tiêu chuẩn là bao nhiêu?
A. Thể tích CO2 là 16,8 lít.
B. Thể tích CO2 là 44,8 lít.
C. Thể tích CO2 là 22,4 lít.
D. Thể tích CO2 là 17,92 lít.
Đáp án: Chọn D. Thể tích CO2 thu được ở điều kiện tiêu chuẩn là 17,92 lít.
