Nguyên tử khối trung bình không phải là con số đo chính xác của khối lượng một nguyên tử. Thay vào đó, đây là khối lượng trung bình mỗi nguyên tử được tính từ một mẫu điển hình của nguyên tố. Nếu bạn có thể đo khối lượng của hàng tỷ nguyên tử riêng lẻ, bạn có thể tìm được giá trị này bằng cách tính giá trị trung bình của chúng. Chúng ta có một phương pháp thực tế hơn, đó là dựa vào thông tin của các đồng vị khác nhau của nguyên tố hóa học.
Quy trình
Tính nguyên tử khối trung bình
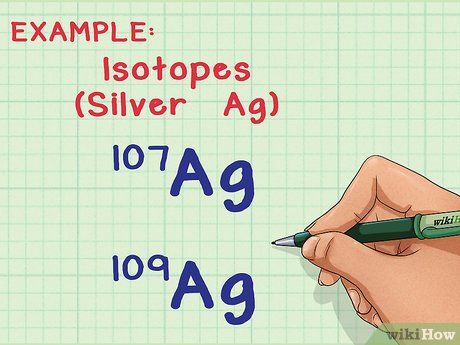
- Ví dụ, nguyên tố bạc (Ag) có hai đồng vị trong tự nhiên: Ag-107 và Ag-109 (hay 107Ag và 109Ag). Đồng vị được đặt tên theo “số khối”, hoặc tổng của số proton và số nơtron trong một nguyên tử. Nghĩa là Ag-109 có nhiều hơn hai nơtron so với Ag-107, do đó nguyên tử của nó nặng hơn một chút.
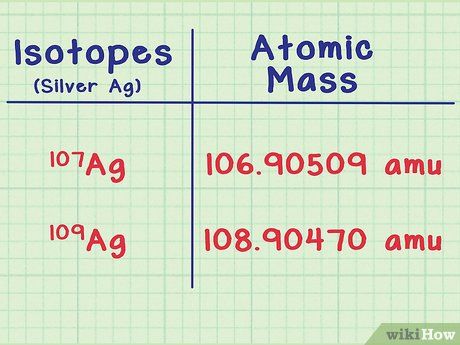



Sử dụng kết quả
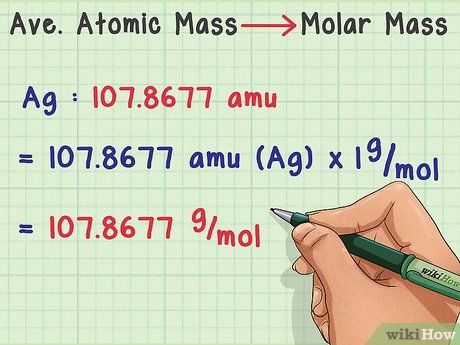

- Một phân tử nước H2O chứa hai nguyên tử hiđro (H) và một nguyên tử oxi (O).
- Hiđro có nguyên tử khối trung bình là 1,00794 amu. Oxi có nguyên tử khối trung bình là 15,9994 amu.
- Vậy khối lượng phân tử trung bình của H2O là (1,00794)(2) + 15,9994 = 18,01528 amu, tương đương với 18,01528 g/mol.
Gợi ý
- Khái niệm khối lượng nguyên tử tương đối đôi khi được sử dụng thay thế cho nguyên tử khối trung bình. Có sự khác biệt nhỏ vì khối lượng nguyên tử tương đối không có đơn vị; đó là phép đo khối lượng so với nguyên tử cacbon-12. Miễn là bạn sử dụng đơn vị khối lượng nguyên tử trong tính toán nguyên tử khối trung bình, hai giá trị này là như nhau.
- Con số trong ngoặc đơn sau nguyên tử khối chỉ ra độ chính xác. Ví dụ, nguyên tử khối 1,0173 (4) biểu thị rằng nguyên tử bình thường của nguyên tố đó có khối lượng dao động trong khoảng 1,0173 ± 0,0004. Bạn không cần phải lấy con số này nếu không cần thiết.
- Trên bảng tuần hoàn, nguyên tử khối trung bình của nguyên tố sau sẽ lớn hơn nguyên tố trước đó, trừ vài trường hợp ngoại lệ. Điều này giúp kiểm tra kết quả của bạn một cách nhanh chóng.
- 1 đơn vị khối lượng nguyên tử bằng 1/12 khối lượng của một nguyên tử cacbon-12.
- Tỷ lệ tồn tại của các đồng vị được tính theo mẫu điển hình tự nhiên. Tuy nhiên, các chất không tồn tại tự nhiên như thiên thạch hoặc được tạo ra trong phòng thí nghiệm có thể có tỷ lệ đồng vị khác nhau, làm cho nguyên tử khối trung bình cũng khác nhau.
Cảnh báo
- Nguyên tử khối luôn được ghi bằng đơn vị khối lượng nguyên tử (amu hoặc u), đôi khi còn được gọi là dalton (Da). Không bao giờ thêm một đơn vị khối lượng khác (như kilogram) sau con số này mà không sửa đổi nó.
Cần chuẩn bị những gì?
- Bút chì
- Giấy
- Máy tính cầm tay
- Dữ liệu về tỷ lệ tồn tại của đồng vị trong tự nhiên.
- Dữ liệu về đơn vị nguyên tử khối của đồng vị.
