

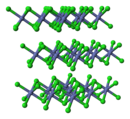
| Cobalt(II) chloride | |||
|---|---|---|---|
|
| |||
|
| |||
| Danh pháp IUPAC | Cobalt(II) chloride | ||
| Tên khác | Cobaltơ chloride Cobalt dichloride Muriat của cobalt | ||
| Nhận dạng | |||
| Số CAS | 7646-79-9 | ||
| PubChem | 3032536 | ||
| Số EINECS | 231-589-4 | ||
| ChEBI | 35696 | ||
| Số RTECS | GF9800000 | ||
| Ảnh Jmol-3D | ảnh | ||
| SMILES | đầy đủ | ||
| InChI | đầy đủ | ||
| ChemSpider | 22708 | ||
| UNII | EVS87XF13W | ||
| Thuộc tính | |||
| Công thức phân tử | CoCl2 | ||
| Khối lượng mol | 129,8384 g/mol (khan) 147,85368 g/mol (1 nước) 165,86896 g/mol (2 nước) 237,9008 g/mol (6 nước) | ||
| Bề ngoài | tinh thể màu chàm (khan) chất rắn màu chàm (2 nước) tinh thể màu hoa hồng (6 nước) | ||
| Khối lượng riêng | 3,356 g/cm³ (khan) 2,477 g/cm³ (2 nước) 1,924 g/cm³ (6 nước) | ||
| Điểm nóng chảy | 735 °C (1.008 K; 1.355 °F) (khan) 140 °C (284 °F; 413 K) (1 nước) 100 °C (212 °F; 373 K) (2 nước) 86 °C (187 °F; 359 K) (6 nước) | ||
| Điểm sôi | 1.049 °C (1.322 K; 1.920 °F) | ||
| Độ hòa tan trong nước | 43,6 g/100 mL (0 ℃) 45 g/100 mL (7 ℃) 52,9 g/100 mL (20 ℃) 105 g/100 mL (96 ℃) | ||
| Độ hòa tan | 38,5 g/100 mL (metanol) 8,6 g/100 mL (aceton) hòa tan trong etanol, pyridin, glixerol tạo phức với nhiều phối tử vô cơ và hữu cơ | ||
| MagSus | +12,660·10 cm³/mol | ||
| Cấu trúc | |||
| Cấu trúc tinh thể | CdCl2 | ||
| Tọa độ | Lục phương (khan) Đơn nghiêng (2 nước) Bát diện (6 nước) | ||
| Các nguy hiểm | |||
| Phân loại của EU | Độc (T) Carc. Cat. 2 Nguy hiểm đối với môi trường (N) | ||
| NFPA 704 |
0
2
0
| ||
| Chỉ dẫn R | R49, R60, R22, R42/43, R68, R50/53 | ||
| Chỉ dẫn S | S53, S45, S60, S61 | ||
| Điểm bắt lửa | không bắt lửa | ||
| LD50 | 80 mg/kg (đường miệng, chuột) | ||
| Các hợp chất liên quan | |||
| Anion khác | Cobalt(II) fluoride Cobalt(II) bromide Cobalt(II) iodide | ||
| Cation khác | Rhodi(III) chloride Iridi(III) chloride | ||
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa).
(cái gì ?)
Tham khảo hộp thông tin | |||
Clorua Cobalt(II) là một hợp chất vô cơ của cobalt và clo, với công thức hóa học CoCl2. Thường xuất hiện dưới dạng ngậm 6 nước CoCl2·6H2O, đây là muối cobalt phổ biến nhất trong các phòng thí nghiệm.
Dạng ngậm 6 nước có màu tím, trong khi dạng khan của nó có màu xanh da trời. Vì dễ dàng hấp thụ hoặc mất nước, và sự thay đổi màu sắc tương ứng, clorua cobalt(II) được sử dụng làm chỉ thị độ ẩm trong các chất chống ẩm.
Clorua cobalt(II) được ứng dụng trong tổng hợp hữu cơ và chế tạo các thiết bị điện cực bằng kim loại cobalt.
Clorua cobalt(II) đã được Cơ quan Hóa chất châu Âu phân loại là chất có nguy cơ nghi ngờ gây ung thư.
Tổng hợp
Cobalt(II) chloride ngậm nước được tạo ra bằng cách cho cobalt(II) carbonate hoặc muối cobalt(II) phản ứng với acid chlorhydric:
- CoCO3 + 2HCl + 5H2O → Co(H2O)6Cl2 + CO2↑
Khi nung nóng, phân tử ngậm 6 phân tử nước sẽ bị phân hủy thành muối khan.
Phản ứng
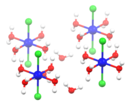
Nhìn chung, dung dịch của các muối này tương tự như các muối cobalt(II) khác, với sự hiện diện của ion [Co(H2O)6]. Khi phản ứng với H2S, các dung dịch muối này sẽ tạo ra kết tủa CoS. CoCl2·6H2O và CoCl2 là các acid Lewis yếu. Các phân tử thường có cấu trúc bát diện hoặc tứ diện. Khi kết hợp với pyridin (C5H5N), chúng tạo thành phức chất bát diện.
- CoCl2·6H2O + 4C5H5N → CoCl2(C5H5N)4 + 6H2O
Khi sử dụng triphenylphosphin (P(C6H5)3), sẽ tạo ra phức chất tứ diện.
- CoCl2·6H2O + 2P(C6H5)3 → CoCl2[P(C6H5)3]2 + 6H2O
Hợp chất khác
CoCl2 có thể tạo ra một số hợp chất với NH3, như CoCl2·2NH3 (hoa hồng), CoCl2·3NH3 (hoa hồng đỏ), CoCl2·4NH3 (vàng nâu), CoCl2·5NH3 (đỏ cam), CoCl2·6NH3 (rơm) và CoCl2·10NH3 (vàng nâu).
CoCl2 cũng tạo ra một số hợp chất với N2H4, ví dụ như CoCl2·6N2H4 là chất rắn màu hồng, dễ nổ và không ổn định. Các hợp chất khác như CoCl2·3N2H4 có màu cam nhạt, CoCl2·2,5N2H4·H2O là tinh thể hồng, và CoCl2·2N2H4 có dạng monohydrat là tinh thể màu đỏ-hồng, tan trong nước và H2SO4/HNO3. CoCl2·1,5N2H4·H2O là tinh thể màu hồng, CoCl2·¾N2H4 và CoCl2·¼N2H4 đều có màu dương nhạt-hồng.
CoCl2 cũng tạo ra một số hợp chất với NH2OH, ví dụ như CoCl2·2NH2OH là tinh thể màu hoa hồng.
CoCl2 có khả năng tạo hợp chất với CO(NH2)2, như CoCl2·2CO(NH2)2 là tinh thể màu đen, CoCl2·4CO(NH2)2 có màu oải hương-hoa hồng và CoCl2·10CO(NH2)2 là tinh thể màu hồng.
CoCl2 cũng tạo ra một số hợp chất với CON3H5, ví dụ như CoCl2·2CON3H5 là tinh thể đỏ, có khả năng hòa tan vừa phải trong nước.
CoCl2 cũng hình thành một số hợp chất với CON4H6, chẳng hạn như CoCl2·2CON4H6·1,5H2O, là tinh thể màu hồng đậm.
CoCl2 tạo ra một số hợp chất với CS(NH2)2, ví dụ như CoCl2·2CS(NH2)2 có màu lục lam, CoCl2·3CS(NH2)2 là chất rắn màu dương, hòa tan trong nước tạo dung dịch màu dương đen, CoCl2·3,5CS(NH2)2 là tinh thể màu dương đen, và CoCl2·4CS(NH2)2 có màu lam dương.
CoCl2 còn tạo ra các hợp chất với CSN3H5, ví dụ như CoCl2·2CSN3H5 là bột hoặc tinh thể màu đen tím, và CoCl2·3CSN3H5·H2O là tinh thể màu đỏ nhạt-hồng.
CoCl2 cũng tạo hợp chất với CSN4H6, trong đó CoCl2·2CSN4H6 có thể xuất hiện dưới dạng tinh thể màu tím hoặc màu nâu.
CoCl2 có thể tạo ra các hợp chất với CSe(NH2)2, chẳng hạn như CoCl2·2CSe(NH2)2 có màu lục lam, và CoCl2·4CSe(NH2)2 có màu lục nhạt. Phức CoCl2·3CSe(NH2)2 có màu khác so với các phức hợp này.
Ứng dụng
- Mực vô hình
- Cobalt(II) chloride là chất kích thích hóa học, có tác dụng tương tự như khi cơ thể bị thiếu oxy, góp phần vào quá trình sinh hồng cầu. Việc bổ sung cobalt không bị cấm và không thể phát hiện qua các bài kiểm tra chống doping hiện tại. Tuy nhiên, cobalt(II) chloride bị cấm theo quy định của Australian Thoroughbred Racing.
Liên kết ngoài
- International Chemical Safety Card 0783
- National Pollutant Inventory – Tờ thông tin về Cobalt Lưu trữ 2006-02-19 tại Wayback Machine
- IARC Monograph 'Cobalt và các hợp chất của Cobalt'
Hợp chất cobalt |
|---|
- Cổng thông tin Hóa học
