
| Kẽm chloride | |
|---|---|
Mẫu kẽm chloride ngậm nước | |
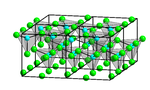
Cấu trúc của kẽm chloride | |
| Danh pháp IUPAC | Zinc chloride |
| Tên khác | Kẽm(II) chloride Kẽm đichloride "Kẽm bơ" Kẽm muriat |
| Nhận dạng | |
| Số CAS | 7646-85-7 |
| PubChem | 3007855 |
| Số EINECS | 231-592-0 |
| ChEBI | 49976 |
| ChEMBL | 1200679 |
| Số RTECS | ZH1400000 |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ |
| InChI | đầy đủ |
| ChemSpider | 5525 |
| UNII | 86Q357L16B |
| Thuộc tính | |
| Công thức phân tử | ZnCl2 |
| Khối lượng mol | 136,2954 g/mol (khan) 154,31068 g/mol (1 nước) 163,31832 g/mol (1,5 nước) 181,3336 g/mol (2,5 nước) 190,34124 g/mol (3 nước) 208,35652 g/mol (4 nước) 298,43292 g/mol (9 nước) |
| Bề ngoài | chất rắn tinh thể màu trắng hút ẩm và dễ chảy nước |
| Mùi | không mùi |
| Khối lượng riêng | 2,907 g/cm³ |
| Điểm nóng chảy | 290 °C (563 K; 554 °F) |
| Điểm sôi | 732 °C (1.005 K; 1.350 °F) |
| Độ hòa tan trong nước | 432 g/100 mL (25 ℃), xem thêm bảng độ tan |
| Độ hòa tan | hòa tan trong etanol, glycerol và aceton tạo phức với nhiều phối tử vô cơ và hữu cơ |
| Độ hòa tan trong cồn | 430 g/100 mL |
| MagSus | -65,0·10 cm³/mol |
| Cấu trúc | |
| Tọa độ | Tứ diện, tuyến tính khi ở dạng khí |
| Dược lý học | |
| Các nguy hiểm | |
| Phân loại của EU | Rất độc (T+) Ăn mòn (C) Nguy hiểm cho môi trường (N) |
| NFPA 704 |
0
3
0
|
| Chỉ dẫn R | R22, R34, R50/53 |
| Chỉ dẫn S | (S1/2), S26, S36/37/39, S45, S60, S61 |
| PEL | TWA 1 mg/m³ (khói) |
| LC50 | 1260 mg/m³ (chuột, 30 phút) 1180 mg-min/m³ |
| LD50 | 350 mg/kg (đường miệng, chuột) 350 mg/kg (chuột, oral) 200 mg/kg (guinea pig, oral) 1100 mg/kg (đường miệng, chuột) 1250 mg/kg (chuột, oral) |
| REL | TWA 1 mg/m³ ST 2 mg/m³ (khói) |
| IDLH | 50 mg/m³ (khói) |
| Các hợp chất liên quan | |
| Anion khác | Kẽm fluoride Kẽm bromide Kẽm iodide |
| Cation khác | Cadmi(II) chloride Thủy ngân(II) chloride |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa).
(cái gì ?)
Tham khảo hộp thông tin | |
Clorua kẽm là tên gọi của các hợp chất có công thức hóa học ZnCl2 và các dạng ngậm nước của chúng. Clorua kẽm, với khả năng ngậm tối đa 9 phân tử nước, xuất hiện dưới dạng chất rắn không màu hoặc trắng, rất dễ tan trong nước. ZnCl2 có tính hút ẩm mạnh và dễ dàng chuyển thành dạng lỏng. Vì vậy, các mẫu của muối này cần được bảo quản tránh tiếp xúc với độ ẩm, bao gồm cả hơi nước trong không khí. Clorua kẽm được sử dụng rộng rãi trong xử lý vải, luyện kim và tổng hợp hóa học. Không có khoáng chất nào chứa thành phần hóa học này, ngoại trừ simonkolleit, một khoáng chất hiếm chứa muối kiềm của clorua kẽm, với công thức Zn5(OH)8Cl2·H2O.
Cấu trúc và đặc tính
ZnCl2 có bốn dạng tinh thể (đa hình): α, β, γ và δ. Trong mỗi dạng đa hình, các ion Zn đều liên kết tứ diện với 4 nguyên tử clo.
Phương pháp điều chế và tinh chế
ZnCl2 khan có thể được tổng hợp từ kẽm và axit clohydric.
- Zn (r) + 2 HCl → ZnCl2 + H2 (k)
Các dạng hydrat và dung dịch nước của ZnCl2 có thể được tạo ra bằng cách cho kẽm kim loại phản ứng với axit clohydric. Kẽm oxit và kẽm sulfide cũng phản ứng với HCl:
- ZnS (rắn) + HCl (dung dịch) → ZnCl2 (dung dịch) + H2S (bay hơi)
Khác với nhiều nguyên tố khác, kẽm chủ yếu chỉ tồn tại trong một trạng thái oxy hóa là +2, điều này giúp đơn giản hóa quá trình tinh chế chloride.
Các mẫu kẽm chloride thương mại thường chứa nước và các tạp chất từ quá trình thủy phân. Để tinh chế, các mẫu này có thể được kết tinh lại từ đioxan nóng. Các mẫu khan có thể được tinh chế bằng cách thăng hoa trong dòng khí hydro chloride, sau đó làm nóng đến 400 ℃ trong dòng khí nitơ. Phương pháp đơn giản nhất là xử lý kẽm chloride với thionyl chloride.
Các hợp chất khác
ZnCl2 còn tạo ra một số hợp chất với NH3, chẳng hạn như ZnCl2·NH3 là tinh thể trắng, ZnCl2·2NH3 là bột không màu, ZnCl2·4NH3 là bột trắng, ZnCl2·5NH3·H2O là tinh thể trắng dễ chảy, hoặc ZnCl2·6NH3 là chất rắn màu trắng.
ZnCl2 cũng tạo một số hợp chất với N2H4, chẳng hạn như ZnCl2·2N2H4 là chất rắn màu trắng.
ZnCl2 còn kết hợp với NH2OH để tạo ra một số hợp chất, ví dụ như ZnCl2·2NH2OH là chất rắn màu trắng.
ZnCl2 cũng tạo ra một số hợp chất với CO(NH2)2, ví dụ ZnCl2·2CO(NH2)2 là tinh thể không màu, với mật độ D = 1,91 g/cm³.
ZnCl2 phản ứng với CON3H5 để tạo ra các hợp chất như ZnCl2·CON3H5 và ZnCl2·2CON3H5, cả hai đều là tinh thể không màu, với mật độ D = 2,08 g/cm³.
ZnCl2 cũng kết hợp với CON4H6 để tạo ra hợp chất ZnCl2·2CON4H6, là tinh thể không màu.
ZnCl2 tạo một số hợp chất với CS(NH2)2, như ZnCl2·2CS(NH2)2 là tinh thể không màu, với mật độ đo được là 1,976 g/cm³ và tính toán là 1,978 g/cm³.
ZnCl2 còn tạo ra hợp chất với CSN3H5, ví dụ ZnCl2·CSN3H5 là tinh thể không màu với mật độ D = 2,25 g/cm³, hoặc ZnCl2·2CSN3H5 là tinh thể trắng, nóng chảy ở 145 °C (293 °F; 418 K).
ZnCl2 cũng phản ứng với CSN4H6 để tạo hợp chất ZnCl2·2CSN4H6, là tinh thể không màu.
ZnCl2 kết hợp với CSeN3H5 tạo ra ZnCl2·CSeN3H5, tinh thể trắng, tan trong nước và cồn, nhưng không tan trong etanol.
ZnCl2 cũng tạo hợp chất với CSeN4H6, ví dụ ZnCl2·2CSeN4H6 là tinh thể không màu.
Tài liệu tham khảo
- N. N. Greenwood, A. Earnshaw, Hóa học các nguyên tố, xuất bản lần 2, Butterworth-Heinemann, Oxford, UK, 1997.
- Lide, D. R. (biên tập) (2005). Sổ tay Hóa học và Vật lý (ấn bản 86). Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5.
- Chỉ mục Merck, xuất bản lần 7, Merck & Co, Rahway, New Jersey, USA, 1960.
- D. Nicholls, Các phức hợp và Nguyên tố chuyển tiếp hàng đầu, Macmillan Press, London, 1973.
- J. March, Hóa học Hữu cơ Nâng cao, xuất bản lần 4, tr. 723, Wiley, New York, 1992.
- G. J. McGarvey, trong Sổ tay các thuốc thử cho Tổng hợp Hữu cơ, Tập 1: Thuốc thử, Phụ gia và Xúc tác cho Sự hình thành Liên kết C-C, (R. M. Coates, S. E. Denmark, biên tập), tr. 220–3, Wiley, New York, 1999.
Liên kết bổ sung
- Phân loại và Ứng dụng của Kẽm Clorua
- Tóm tắt PubChem ZnCl2
Hợp chất kẽm |
|---|
- Thư viện Hóa học
