| Acid và base |
|---|
|
| Các dạng acid |
|
| Các dạng base |
|
- Với từng acid hoặc base yếu, xin xem bài Tác nhân đệm. Với những bài viết không liên quan đến acid-base hoá học, xin xem Đệm (định hướng).
Dung dịch đệm là một loại dung dịch lỏng chứa một hỗn hợp acid yếu và base liên hợp hoặc base yếu và acid liên hợp. Tính chất đặc biệt của dung dịch này là khi thêm một lượng chất có tính base hay acid, pH của dung dịch thay đổi rất ít so với ban đầu. Dung dịch đệm được ứng dụng rộng rãi trong ngành thí nghiệm và tự nhiên để duy trì độ pH ổn định.
Lý thuyết
Trong dung dịch acid yếu luôn tồn tại một cân bằng giữa phân tử acid và base liên hợp của nó, được biểu diễn như sau:
- HA + H2O ⇌ H3O + A
Khi thêm ion H vào dung dịch, cân bằng sẽ dịch chuyển về phía bên trái theo nguyên lý dịch chuyển Le Chatelier; và cân bằng sẽ dịch chuyển sang phía phải nếu ion H trong dung dịch giảm theo phản ứng H + OH → H2O. Do đó, khi có tác động, cân bằng mới sẽ thiết lập và làm thay đổi pH.
Hằng số phân ly acid HA được định nghĩa bằng biểu thức sau đây:
Dùng một số thao tác biến đổi logarit ta có phương trình Henderson-Hasselbalch, trong đó pH phụ thuộc vào pKa
Gọi [A] là nồng độ của base liên hợp, [HA] là nồng độ của acid yếu tại thời điểm cân bằng được thiết lập. Ta có được đẳng thức pH=pKa khi nồng độ của acid và base liên hợp bằng nhau, thường được gọi là bán trung hoà. Nhìn chung, việc tính toán pH của dung dịch đệm không khó khăn, chỉ cần biết các chất trong hỗn hợp, xem bảng Bắt đầu-Phản ứng-Cân bằng (hay còn gọi là ICE table).
Nên lưu ý, việc đo độ pH và tính toán pH không giống nhau. Điện cực thủy tinh điện sử dụng trong hầu hết các máy đo pH, điện cực này không chỉ dựa vào nồng độ ion hydro mà còn dựa vào hoạt tính của riêng nó do nhiều yếu tố gây ra, chủ yếu là độ mạnh ion của môi trường. Ví dụ, tính pH của dung dịch đệm phosphat thì được giá trị 7,96 nhưng pH thực lại là 7,4.
Xét tiếp ví dụ trên cho trường hợp base yếu (B) và acid liên hợp (BH).
- B + H2O ⇌ BH + OH.
Giá trị pKa được sử dụng cho acid liên hợp với base trên.
Nhìn chung, một dung dịch đệm có thể được tạo thành từ nhiều hơn một acid yếu và các base liên hợp của nó; ta có thể tạo ra một vùng đệm rộng hơn vùng đệm ban đầu bằng cách trộn các tác nhân đệm riêng lẻ.
Khả năng đệm
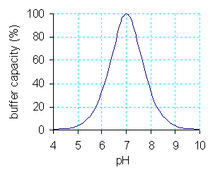
Độ đệm là một đại lượng định lượng được sử dụng để đo lường mức độ dung dịch cản trở quá trình thay đổi pH khi cho ion hydroxid vào. Nó được định nghĩa bằng công thức sau.
- Độ đệm =
trong đó dn là lượng baseơ biến thiên rất nhỏ và kéo theo d(pH) là sự thay đổi pH rất nhỏ. Với định nghĩa này, độ đệm có thể được biểu diễn bằng công thức
với Kw là hằng số tự ion hoá của nước và CA là nồng độ acid ghi nhận được, bằng với [HA]+[A]. Cụm Kw/[H] đóng vai trò quan trọng khi pH lớn hơn 11,5 và cụm kế đóng vai trò quan trọng khi pH nhỏ hơn khoảng 2. Cả hai đều là những đặc trưng của nước và không phụ thuộc vào acid yếu. Xét cụm còn lại, ta thấy
- Độ đệm của acid yếu đạt cực đại khi giá trị pH = pKa
- Tại pH = pKa ± 1 độ đệm giảm còn lại 33% giá trị cực đại. Đây là khoảng xấp xỉ nằm trong vùng đệm hiệu quả của acid yếu. Ghi chú: khi pH = pKa - 1, phương trình Henderson-Hasselbalch cho ta kết quả [HA]:[A] bằng 10:1.
- Độ đệm tỉ lệ trực tiếp với nồng độ ghi nhận được của acid.
Ứng dụng của dung dịch đệm
Khả năng chống lại sự thay đổi đột ngột của pH giúp dung dịch đệm được sử dụng rộng rãi trong các quá trình hóa học và là yếu tố quan trọng cho các chu trình sinh hóa. Để có một dung dịch đệm lý tưởng cho một pH nhất định, con số pKa cần phải bằng với pH, từ đó tạo nên dung dịch đệm hiệu quả nhất.
Dung dịch đệm giúp duy trì độ pH ổn định cho các enzyme trong cơ thể sống hoạt động. Nhiều enzyme chỉ hoạt động tốt trong điều kiện pH nhất định; nếu pH thay đổi quá mức, enzyme có thể bị ức chế hoặc mất hoạt tính, gây ra tác dụng không mong muốn.
Trong công nghiệp, dung dịch đệm được sử dụng trong các quá trình lên men và cũng được áp dụng trong phân tích hóa học và chuẩn độ pH.
Hầu hết các mẫu sinh học được nghiên cứu trong dung dịch đệm PBS (phosphate buffered saline) với pH 7.4, một loại dung dịch đệm đặc biệt.
Hỗn hợp dung dịch đệm
Chất Khoảng pH HCl, Natri citrat 1 - 5 Acid citric , Natri citrat 2,5 - 5,6 Acid acetic, Natri acetat 3,7 - 5,6 Na2HPO4, NaH2PO4 6 - 9 Borax, Natri hydroxide 9,2 - 11
Hỗn hợp đa dụng
Bằng cách kết hợp các chất tan có các pKa khác nhau khoảng 2 đơn vị, ta có thể tạo ra dung dịch đệm có khả năng đệm rộng. Acid citric là một trong những hợp chất được sử dụng phổ biến vì có 3 nấc pKa. Khoảng đệm có thể mở rộng hơn tùy thuộc vào chất phụ gia. Hỗn hợp dưới đây cung cấp một khoảng đệm từ pH 3 đến 8.
0,2M Na2HPO4/mL 0,1M Acid citric/mL pH... 20,55 79,45 3,0 38,55 61,45 4,0 51,50 48,50 5,0 63,15 36,85 6,0 82,35 17,65 7,0 97,25 2,75 8,0
Hỗn hợp bao gồm acid citric, kali dihydrophosphat, acid boric và acid diethyl barbituric có thể cung cấp một khoảng đệm từ pH 2,6 đến 12.
Các hợp chất đệm sinh học phổ biến
| Tên thường | pKa tại 25 °C |
Khoảng đệm | Tác động nhiệt d(pH)/dT trong (1/K) ** |
Khối lượng mol | Tên đầy đủ |
|---|---|---|---|---|---|
| TAPS | 8,43 | 7,7-9,1 | −0,018 | 243,3 | acid 3-{[tri(hydroxymetyl)methyl]amino}propansulfonic |
| Bicine | 8,35 | 7,6-9,0 | −0,018 | 163,2 | N,N-bis(2-hydroxyetyl)glycin |
| Tris | 8,06 | 7,5-9,0 | −0,028 | 121,14 | tri(hydroxymetyl)metylamin |
| Tricine | 8,05 | 7,4-8,8 | −0,021 | 179,2 | N-tri(hydroxymetyl)metylglycin |
| HEPES | 7,48 | 6,8-8,2 | −0,014 | 238,3 | acid 4-2-hydroxyetyl-1-piperazineetansulfonic |
| TES | 7,40 | 6,8-8,2 | −0,020 | 229,20 | acid 2-{[tri(hydroxymetyl)metyl]amino}etansulfonic |
| MOPS | 7,20 | 6,5-7,9 | −0,015 | 209,3 | acid3-(N-morpholino)propansulfonic |
| PIPES | 6,76 | 6,1-7,5 | −0,008 | 302,4 | piperazine-N,N′-bi(acid 2-etansulfonic) |
| Cacodylate | 6,27 | 5,0-7,4 | 138,0 | acid dimetylarsinic | |
| MES | 6,15 | 5,5-6,7 | −0,011 | 195,2 | acid 2-(N-morpholino)etansulfonic |
** Các giá trị được xấp xỉ.
- Tác nhân đệm
- Đệm tốt
- Hiệu ứng ion chung
- Liên kết đến các nguồn hóa chất bên ngoài
Chú thích
Liên kết ngoài
- Giải pháp đệm
- Phương trình Henderson-Hasselbalch và thảo luận về công thức
- Bài giảng video về đệm tại Đại học UC Berkeley
- Phần mềm tính toán miễn phí cho việc tính toán pH, phân bố các chất và chuẩn độ đệm (khả năng đệm)
- Công cụ tính toán đệm Sigma Aldrich - Công cụ hữu ích để tính toán trọng lượng, thể tích hoặc nồng độ từ khối lượng phân tử.
Vấn đề liên quan đến dung dịch | |
|---|---|
| Dung dịch | Dung dịch lý tưởng • Dung dịch đệm• Dung dịch lỏng • Dung dịch rắn • Flory-Huggins • Hỗn hợp • Huyền phù • Dung dịch keo • Giản đồ pha • Eutecti • Hợp kim |
| Nồng độ | Bão hòa (hóa học) • Quá bão hòa • Molar solution • Percentage solution • Serial dilution |
| Độ hòa tan | Cân bằng tan • Tổng chất rắn hòa tan • Solvat hóa • Solvation shell • Biến thiên Enthalpy trong dung dịch • Năng lượng mạng tinh thể • Định luật Raoult • Định luật Henry • Bảng độ tan (giá trị) • Bảng tính tan |
| Dung môi | (thể loại) • Hằng số điện ly axit • Dung môi proton • Dung môi vô cơ • Solvat hóa
Bảng giá trị nghiệm sôi và lạnh của các dung môi • Hệ số phân tán • Độ phân cực • Chất ưa nước • Chất kị nước • Ưa béo • Ưa nước và chất béo |
