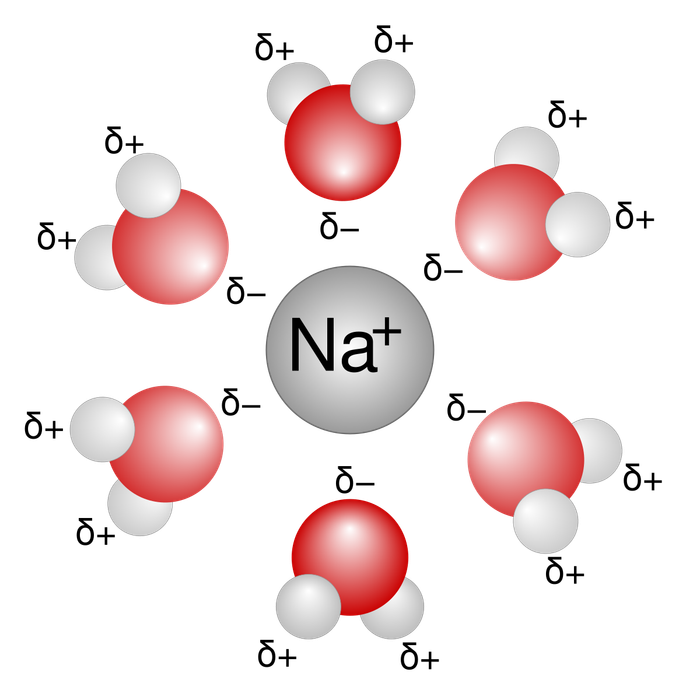
Dung dịch nước là loại dung dịch mà trong đó dung môi chính là nước. Trong các phương trình hóa học, nó thường được ký hiệu bằng cách thêm (aq) vào công thức hóa học tương ứng. Ví dụ, dung dịch muối hay natri chloride trong nước sẽ được viết là Na+ Cl.
Chất kỵ nước thường không tan trong nước, ngược lại, các chất ưa nước lại hòa tan tốt trong nước. Một ví dụ về chất ưa nước là natri chloride. Acid và base cũng là dung dịch nước, đóng vai trò trong các phản ứng acid–base.
Khả năng hòa tan của một chất trong nước phụ thuộc vào khả năng của nó trong việc vượt qua hoặc hòa hợp với các lực hấp dẫn mạnh mẽ giữa các phân tử nước. Nếu chất không hòa tan tốt, nó sẽ tạo thành kết tủa.
Trong dung dịch nước, phản ứng thường xảy ra là phản ứng trao đổi. Phản ứng trao đổi, hay còn gọi là phản ứng dịch chuyển kép, xảy ra khi một ion cation di chuyển và hình thành liên kết với một anion khác. Cation mới liên kết với anion thứ hai sẽ bị tách ra và kết hợp với anion khác.
Dung dịch nước có khả năng dẫn điện tốt khi chứa các chất điện phân mạnh, trong khi các chất dẫn điện kém là các chất điện phân yếu. Các chất điện phân mạnh hoàn toàn ion hóa trong nước, còn các chất điện phân yếu chỉ tạo ra một lượng ion hóa nhỏ.
Dung dịch không điện phân là các chất hòa tan trong nước nhưng vẫn giữ nguyên cấu trúc phân tử của chúng mà không phân tách thành ion. Ví dụ về các chất này bao gồm đường, ure, glycerin và methylsulfonylmethan (MSM).
Khi viết phương trình phản ứng cho dung dịch nước, cần xác định lượng kết tủa. Để làm điều này, người ta tham khảo biểu đồ độ tan. Các hợp chất hòa tan sẽ tạo dung dịch nước, trong khi hợp chất không tan sẽ tạo thành kết tủa.
Khi thực hiện các tính toán liên quan đến phản ứng của một hoặc nhiều dung dịch nước, cần biết nồng độ của dung dịch, tức là số mol của chất tan trước khi hòa tan. Nồng độ dung dịch được biểu diễn dưới dạng chất tan ban đầu.
- Cation kim loại trong dung dịch
- Hòa tan
- Phân ly hóa học
- Phản ứng giữa axit và bazơ
- Đặc tính của nước
- Zumdahl S. Năm 1997. Hóa học. Tái bản lần thứ 4. Boston: Houghton Mifflin Company. Trang 133-145.
