 FDA đã chấp thuận cho công ty Wandercraft sử dụng thiết bị khung xương điện tử (exoskeleton) mang tên Atalante trong quá trình phục hồi chức năng ở những bệnh nhân mắc đột quỵ tại Mỹ. Sản phẩm này sẽ hỗ trợ các bệnh nhân trong quá trình huấn luyện chuyên sâu về dáng đi, đặc biệt với những người gặp vấn đề về cử động của phần cơ trên.Wandercraft vừa mới bắt đầu hoạt động kinh doanh tại Mỹ. Tuy nhiên, tổ chức Quản lý Quadrant, là nguồn tài chính chính của họ, khẳng định rằng họ có khả năng tăng sản xuất mạnh mẽ cho sản phẩm robot exoskeleton này chỉ trong 1 hoặc 2 năm tới, tuỳ thuộc vào nhu cầu của thị trường.
FDA đã chấp thuận cho công ty Wandercraft sử dụng thiết bị khung xương điện tử (exoskeleton) mang tên Atalante trong quá trình phục hồi chức năng ở những bệnh nhân mắc đột quỵ tại Mỹ. Sản phẩm này sẽ hỗ trợ các bệnh nhân trong quá trình huấn luyện chuyên sâu về dáng đi, đặc biệt với những người gặp vấn đề về cử động của phần cơ trên.Wandercraft vừa mới bắt đầu hoạt động kinh doanh tại Mỹ. Tuy nhiên, tổ chức Quản lý Quadrant, là nguồn tài chính chính của họ, khẳng định rằng họ có khả năng tăng sản xuất mạnh mẽ cho sản phẩm robot exoskeleton này chỉ trong 1 hoặc 2 năm tới, tuỳ thuộc vào nhu cầu của thị trường.
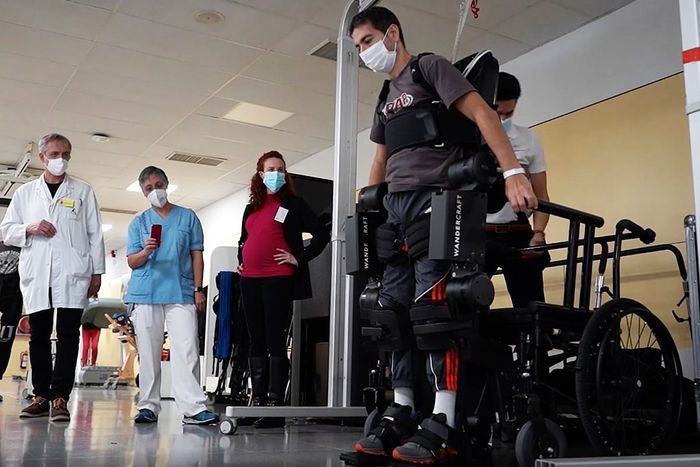 Phiên bản mới nhất của công ty sử dụng pin để loại bỏ sự rắc rối của dây điện, có khả năng tự cân bằng và có thể điều chỉnh dáng đi của bệnh nhân. Hiện tại sản phẩm vẫn cần sự giám sát của kỹ thuật viên và phải hoạt động trong phạm vi phòng khám để dễ dàng quản lý. Tuy nhiên, với khả năng điều chỉnh dáng đi và các công nghệ đã nêu, công ty hy vọng sẽ giúp bệnh nhân có thể phục hồi dáng đi của mình, bất kể họ có thể sử dụng phần tay hay không.
Phiên bản mới nhất của công ty sử dụng pin để loại bỏ sự rắc rối của dây điện, có khả năng tự cân bằng và có thể điều chỉnh dáng đi của bệnh nhân. Hiện tại sản phẩm vẫn cần sự giám sát của kỹ thuật viên và phải hoạt động trong phạm vi phòng khám để dễ dàng quản lý. Tuy nhiên, với khả năng điều chỉnh dáng đi và các công nghệ đã nêu, công ty hy vọng sẽ giúp bệnh nhân có thể phục hồi dáng đi của mình, bất kể họ có thể sử dụng phần tay hay không.
 Cách điều chỉnh dáng đi của AtalanteCho đến thời điểm hiện tại, FDA chỉ mới phê duyệt một số rất ít các sản phẩm tương tự, và nếu phê duyệt, cũng sẽ có các điều kiện rất nghiêm ngặt. Ví dụ, vào tháng 6 năm ngoái, Ekso Bionics đã được phê duyệt cho thiết bị có tên là EksoNR để hỗ trợ phục hồi chức năng cho các bệnh nhân mắc chứng xơ cứng. Việc phê duyệt cho công ty Wandercraft sẽ giúp họ tiếp cận nhóm bệnh nhân lớn hơn so với Ekso Bionics, bởi vì hiện nay mỗi năm có gần 800 nghìn người Mỹ mắc đột quỵ. Dự kiến công ty này sẽ đưa các sản phẩm đầu tiên vào Mỹ ngay trong quý 1 năm nay và chưa tiết lộ ai là những khách hàng đầu tiên của họ.
Cách điều chỉnh dáng đi của AtalanteCho đến thời điểm hiện tại, FDA chỉ mới phê duyệt một số rất ít các sản phẩm tương tự, và nếu phê duyệt, cũng sẽ có các điều kiện rất nghiêm ngặt. Ví dụ, vào tháng 6 năm ngoái, Ekso Bionics đã được phê duyệt cho thiết bị có tên là EksoNR để hỗ trợ phục hồi chức năng cho các bệnh nhân mắc chứng xơ cứng. Việc phê duyệt cho công ty Wandercraft sẽ giúp họ tiếp cận nhóm bệnh nhân lớn hơn so với Ekso Bionics, bởi vì hiện nay mỗi năm có gần 800 nghìn người Mỹ mắc đột quỵ. Dự kiến công ty này sẽ đưa các sản phẩm đầu tiên vào Mỹ ngay trong quý 1 năm nay và chưa tiết lộ ai là những khách hàng đầu tiên của họ.