
| Kali manganat | |
|---|---|
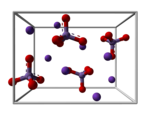
Cấu trúc của kali manganat | |
Mẫu kali manganat | |
| Danh pháp IUPAC | Kali manganat(VI) |
| Tên khác | Kali manganat(VI) |
| Nhận dạng | |
| Số CAS | 10294-64-1 |
| PubChem | 160931 |
| Số EINECS | 233-665-2 |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ |
| InChI | đầy đủ |
| ChemSpider | 141385 |
| UNII | 5PI213D3US |
| Thuộc tính | |
| Công thức phân tử | K2MnO4 |
| Khối lượng mol | 197,1322 g/mol |
| Bề ngoài | tinh thể màu lục đậm |
| Khối lượng riêng | 2,78 g/cm³ |
| Điểm nóng chảy | 190 °C (463 K; 374 °F) (phân hủy) |
| Điểm sôi | |
| Độ hòa tan trong nước | phân hủy |
| Độ axit (pKa) | 7,1 |
| Cấu trúc | |
| Cấu trúc tinh thể | Trực thoi |
| Tọa độ | Cấu trúc anion tứ diện |
| Các nguy hiểm | |
| Nguy hiểm chính | chất oxy hóa |
| NFPA 704 |
0
1
1
|
| Chỉ dẫn R | R8 R36/37/38 |
| Chỉ dẫn S | S17 S26 S36/37/39 |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa).
(cái gì ?)
Tham khảo hộp thông tin | |
Kali manganat là một hợp chất vô cơ với công thức hóa học K2MnO4. Nó có màu xanh lá cây đậm và đóng vai trò là chất trung gian trong việc sản xuất kali pemanganat (KMnO4, còn được gọi là thuốc tím) trong ngành công nghiệp. Mặc dù kali manganat có thể bị nhầm lẫn với kali pemanganat, chúng là những hợp chất khác nhau với những đặc tính rõ rệt.
Cấu trúc
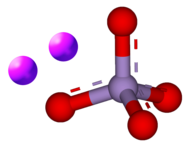
K2MnO4 là một loại muối, bao gồm 2 cation K và anion MnO
4. X-quang tinh thể cho thấy anion có hình dạng tứ diện, với khoảng cách Mn–O là 1,66 Å, dài hơn so với khoảng cách Mn-O trong KMnO4 khoảng 0,04 Å. Nó có cấu trúc tương tự như kali sunfat.
Tổng hợp
Kali manganat có thể được sản xuất công nghiệp bằng cách phản ứng giữa mangan dioxide với kali hydroxide trong môi trường oxy:
- 2MnO2 + 4KOH + O2 → 2K2MnO4 + 2H2O
Trong phòng thí nghiệm, kali manganat có thể được chế tạo bằng cách đun nóng kali pemanganat trong dung dịch kali hydroxide đậm đặc, sau đó làm nguội để thu được tinh thể màu xanh lục đậm của kali manganat:
- 4KMnO4 + 4KOH → 4K2MnO4 + O2 + 2H2O
Có rất ít phản ứng mà trong đó nhóm OH hoạt động như một chất khử. Dung dịch K2MnO4 được tạo ra bằng cách khuấy đều KMnO4 hòa tan trong KOH 5–10 M trong vòng một ngày ở nhiệt độ phòng, sau đó loại bỏ MnO2 không hòa tan.
Để khử một electron từ pemanganat thành manganat, có thể dùng anion I làm chất khử:
- 2KMnO4 + 2KI → 2K2MnO4 + I2
Phản ứng này sẽ thay đổi màu sắc từ tím đặc trưng của pemanganat sang màu xanh lục đậm của manganat. Nó cũng chứng minh rằng pemanganat(VII) có thể hoạt động như một chất nhận electron thay vì chỉ đóng vai trò là chất chuyển oxy. Bari manganat, BaMnO4, được tạo ra bằng cách khử KMnO4 với anion I trong sự hiện diện của bari chloride. Tương tự như BaSO4, BaMnO4 ít tan trong hầu hết các dung môi.
Một cách đơn giản để tổng hợp kali manganat trong phòng thí nghiệm là nung nóng tinh thể hoặc bột kali pemanganat tinh khiết. Kali pemanganat sẽ phân hủy thành kali manganat, mangan(IV) oxit và khí oxy:
- 2KMnO4 → K2MnO4 + MnO2 + O2
Phản ứng này được sử dụng để sản xuất oxy trong phòng thí nghiệm, nhưng kali manganat thu được thường có lẫn mangan dioxide.
Phản ứng
Kali manganat khá bền trong dung dịch kiềm, nhưng nó phân hủy trong nước, tạo ra kali pemanganat và mangan dioxide:
- 3K2MnO4 + 2H2O → 2KMnO4 + MnO2 + 4KOH
Hợp chất kali |
|---|
Hợp chất mangan |
|---|
- Cổng thông tin về Hóa học
