Giải Khoa học tự nhiên 8 Bài 12: Oxide đưa ra câu trả lời cho các học sinh lớp 8 về các câu hỏi thảo luận, và bài tập trang 56, 57, 58, 59, 60 trong sách Chân trời sáng tạo.
Giải KHTN 8 Bài 12: Khám phá sáng tạo giúp học sinh hiểu về khái niệm, tính chất hóa học và ứng dụng của Oxide, đồng thời cung cấp tư liệu cho giáo viên soạn giáo án. Dưới đây là nội dung chi tiết của giải KHTN 8 Bài 12: Oxide.
Giải Khoa học tự nhiên 8 Bài 12: Oxide
Câu hỏi thảo luận KHTN 8 Bài 12: Khám phá sáng tạo
Câu 1
Các thành phần của các hợp chất ở Hình 12.1 có điểm gì tương đồng nhau?

Trả lời:
Điểm tương đồng: Các hợp chất đều chứa 2 nguyên tố, trong đó có 1 nguyên tố là oxygen.
Câu 2
Hãy viết phương trình hóa học của phản ứng trong Ví dụ 2.

Trả lời:
2
Câu 3
Viết phương trình hóa học của phản ứng trong Ví dụ 4.

Trả lời:
 2
2Câu 4
Thành phần của gỉ sét chứa Fe2O3. Từ Ví dụ 5, vì sao giấm ăn có thể làm sạch được gỉ sét trên bề mặt dụng cụ làm bằng sắt – thép?
Trả lời:
Do giấm ăn có tính axit, có thể phản ứng với gỉ sét tạo thành muối tan dễ rửa trôi.
6CH3COOH + Fe2O3 → 2(CH3COO)3Fe + 3H2O.
Câu 5
Khi thực hiện các thí nghiệm với oxide của các kim loại beryllium, chì (lead), chromium (III), chúng đều tan được cả trong dung dịch HCl và dung dịch NaOH. Theo em, các oxide này được gọi là oxide gì?
Trả lời:
Các oxide này là oxide amphoteric vì chúng vừa tan trong dung dịch axit HCl và vừa tan trong dung dịch kiềm NaOH.
Câu 6
Mô tả và viết phương trình hoá học của sự phản ứng xảy ra trong Thí nghiệm 1. Nếu thay dung dịch HCl bằng dung dịch H2SO4, liệu có phản ứng hoá học không? Hãy giải thích.
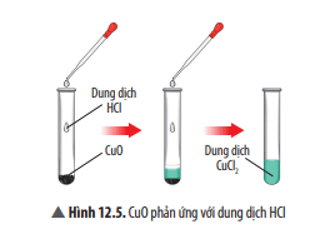
Trả lời:
Hiện tượng: CuO tan dần, sau đó thu được dung dịch màu xanh.
Phương trình hoá học: CuO + 2HCl → CuCl2 + H2O.
Nếu thay HCl bằng H2SO4, phản ứng vẫn xảy ra, vì CuO là oxit bazơ và tác dụng với H2SO4 là axit.
Câu số 7
Quan sát Thí nghiệm 2 (Hình 12.6), mô tả hiện tượng và phản ứng hóa học trong cốc thuỷ tinh.
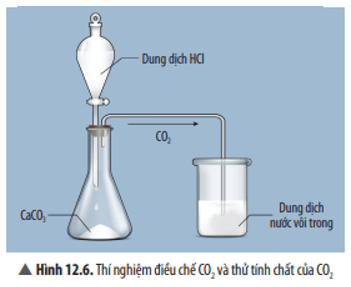
Trả lời:
Hiện tượng: Xuất hiện kết tủa màu trắng.
Phương trình hoá học: CO2 + Ca(OH)2 → CaCO3 + H2O.
Bài 12 - Luyện tập Khoa học tự nhiên 8
Trang 56 của bộ sách Luyện tập
Trong các chất sau, chất nào được xem là oxide: ZnO; SiO2; KNO3; Fe2O3; Cl2O7; K2CO3?
Trả lời:
Chất là oxide: ZnO; SiO2; Fe2O3; Cl2O7.
Luyện tập trang 57
Viết phương trình hoá học giữa khí oxygen và đơn chất tương ứng để tạo ra các oxide sau: Na2O, SO2, ZnO.
Trả lời:
4Na + O2 → 2Na2O
 22
22
Luyện tập trang 58
Cho các loại oxide sau: Fe2O3; SiO2; K2O; SO2; NO2; BaO; CO2; CuO; CaO. Trong số chúng, oxide nào được coi là oxide bazơ, oxide axit?
Trả lời:
Oxide bazơ: Fe2O3; K2O; BaO; CuO; CaO.
Oxide axit: SiO2; SO2; NO2; CO2.
Luyện tập trang 60
Chọn oxide và acid tương ứng, viết phương trình hoá học tạo ra các muối sau:
a) CaCl2. b) MgSO4.
c) FeCl2. d) Fe2(SO4)3.
Trả lời:
a) CaO + 2HCl → CaCl2 + H2O
b) MgO + H2SO4 → MgSO4 + H2O
c) FeO + 2HCl → FeCl2 + H2O
d) Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O.
Luyện tập trang 61
Có các loại oxide: SO3, P2O5, CO, MgO. Oxide nào phản ứng với dung dịch KOH? Oxide nào phản ứng với dung dịch HCl? Viết phương trình hoá học của phản ứng.
