
| Magnesi hydroxide | |
|---|---|
Mẫu magnesi hydroxide | |
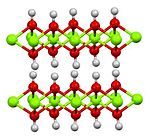
Cấu trúc của magnesi hydroxide | |
| Danh pháp IUPAC | Magnesium hydroxide |
| Tên khác | Sữa magnesi Magnesi dihydroxide |
| Nhận dạng | |
| Số CAS | 1309-42-8 |
| PubChem | 14791 |
| Số EINECS | 215-170-3 |
| ChEBI | 6637 |
| ChEMBL | 1200718 |
| Số RTECS | OM3570000 |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ |
| InChI | đầy đủ |
| Tham chiếu Gmelin | 485572 |
| UNII | NBZ3QY004S |
| Thuộc tính | |
| Công thức phân tử | Mg(OH)2 |
| Khối lượng mol | 58,31968 g/mol |
| Bề ngoài | Chất rắn màu trắng |
| Mùi | Không mùi |
| Khối lượng riêng | 2,3446 g/cm³ |
| Điểm nóng chảy | 350 °C (623 K; 662 °F) (phân hủy) |
| Điểm sôi | |
| Độ hòa tan trong nước |
|
| Tích số tan, Ksp | 5,61×10 |
| MagSus | -22,1·10 cm³/mol |
| Chiết suất (nD) | 1,559 |
| Cấu trúc | |
| Cấu trúc tinh thể | lục phương, hP3 |
| Nhóm không gian | P3m1 No. 164 |
| Hằng số mạng | a = 0,312 nm, c = 0,473 nm |
| Nhiệt hóa học | |
| Enthalpy hình thành ΔfH298 | -924,7 kJ·mol |
| Entropy mol tiêu chuẩn S298 | 64 J·mol·K |
| Nhiệt dung | 77,03J/mol·K |
| Dược lý học | |
| Các nguy hiểm | |
| Nguy hiểm chính | độc |
| NFPA 704 |
0
1
0
|
| Điểm bắt lửa | không cháy |
| LD50 | 8500 mg/kg (chuột cống, miệng) |
| Các hợp chất liên quan | |
| Anion khác | Magnesi oxide |
| Cation khác |
|
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa).
(cái gì ?)
Tham khảo hộp thông tin | |
Magie hydroxide là một hợp chất vô cơ có công thức hóa học Mg(OH)2. Nó xuất hiện tự nhiên trong khoáng chất brucit và có dạng rắn màu trắng với độ hòa tan thấp trong nước (Ksp = 5.61×10). Magie hydroxide thường được sử dụng trong các sản phẩm kháng acid, chẳng hạn như sữa magnesia, và cũng là thành phần của các thuốc nhuận tràng.
Phương pháp điều chế
Để điều chế, ta kết hợp dung dịch muối magnesi với nước nóng, dẫn đến sự hình thành kết tủa rắn Mg(OH)2:
- Mg + 2 OH → Mg(OH)2
Trong sản xuất công nghiệp, Mg(OH)2 được tạo ra bằng cách xử lý nước biển với calci hydroxide (Ca(OH)2). Từ 600 m³ nước biển, có thể thu được khoảng một tấn Mg(OH)2. Vì Ca(OH)2 dễ hòa tan hơn Mg(OH)2, nên magnesi hydroxide sẽ kết tủa thành dạng rắn.
- Mg + Ca(OH)2 → Mg(OH)2 + Ca
Các ứng dụng
Phần lớn Mg(OH)2 được sản xuất công nghiệp, cùng với một lượng nhỏ được khai thác, được chuyển đổi thành magnesi oxide (MgO). Magnesi oxide rất hữu ích vì nó vừa là một chất dẫn điện kém vừa là một chất dẫn nhiệt tốt.
Hợp chất magnesi |
|---|
- Cổng thông tin Hóa học
