| Natri aluminat | |
|---|---|
| Tên khác | Natri aluminium oxide Natri metaaluminate Aluminate, (AlO2), sodium |
| Nhận dạng | |
| Số CAS | 1302-42-7 |
| PubChem | 14766 |
| Số EINECS | 215-100-1 |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ |
| InChI | đầy đủ |
| Thuộc tính | |
| Công thức phân tử | NaAlO2 |
| Khối lượng mol | 81,9688 g/mol (khan) 104,4879 g/mol (5⁄4 nước) |
| Bề ngoài | màu trắng (đôi khi ánh vàng nhạt), ưa ẩm |
| Mùi | không mùi |
| Khối lượng riêng | 1,5 g/cm³ |
| Điểm nóng chảy | 1.650 °C (1.920 K; 3.000 °F) |
| Điểm sôi | |
| Độ hòa tan trong nước | tan được |
| Độ hòa tan | tan trong rượu |
| Chiết suất (nD) | 1,566 |
| Cấu trúc | |
| Cấu trúc tinh thể | Trực thoi |
| Nhiệt hóa học | |
| Enthalpy hình thành ΔfH298 | -1.133,2 kJ/mol |
| Entropy mol tiêu chuẩn S298 | 70,4 J/mol K |
| Nhiệt dung | 73,6 J/mol K |
| Các nguy hiểm | |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). Tham khảo hộp thông tin | |
Natri aluminat là một hóa chất vô cơ quan trọng trong thương mại. Nó hoạt động như nguồn cung cấp nhôm hydroxide hiệu quả cho nhiều ứng dụng công nghiệp và kỹ thuật. Natri aluminat tinh khiết (không có nước) là chất rắn kết tinh màu trắng với các công thức được biết đến là NaAlO2, Na2O·Al2O3, Na2Al2O4 hoặc NaAl(OH)4. Natri aluminat thương mại có thể xuất hiện ở dạng dung dịch hoặc dạng rắn. Các hợp chất khác, đôi khi cũng được gọi là natri aluminat, được tạo ra bằng phản ứng của Na2O và Al2O3, bao gồm Na5AlO4 chứa anion AlO4 riêng biệt, Na7Al3O8 và Na17Al5O16 có chứa các anion phức hợp, và NaAl11O17, từng bị nhầm lẫn là β-alumina, một pha của nhôm oxit.
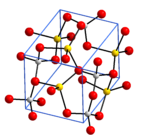
Cấu trúc
Natri aluminat khô, NaAlO2, có cấu trúc ba chiều bao gồm các tứ diện AlO4 liên kết tại các góc. Dạng ngậm nước NaAlO2·5⁄4H2O có cấu trúc lớp với các tứ diện AlO4 kết nối thành vòng, và các lớp được duy trì bằng các ion natri và phân tử nước với hydro liên kết với các nguyên tử oxy trong các tứ diện AlO4.
Sản xuất
Natri aluminat được tạo ra bằng cách hòa tan nhôm hydroxide trong dung dịch NaOH. Gibbsit (nhôm hydroxide) có thể tan trong dung dịch NaOH 20–25% ở nhiệt độ gần sôi. Sử dụng dung dịch NaOH đậm đặc hơn sẽ tạo ra một sản phẩm nửa rắn. Quá trình này cần được thực hiện trong các bình niken hoặc thép đun nóng bằng hơi nước, và nhôm hydroxide phải được đun sôi với dung dịch khoảng 50% NaOH cho đến khi thành dạng bột nhão. Hỗn hợp sau cùng phải được đổ vào thùng và làm nguội; sau đó một khối rắn chứa khoảng 70% NaAlO2 sẽ hình thành. Sau khi nghiền vụn, sản phẩm được sấy khô trong lò quay. Sản phẩm cuối cùng chứa 90% NaAlO2, 1% nước và 1% NaOH tự do.
Phản ứng giữa nhôm kim loại và kiềm
Natri aluminat cũng được tạo thành từ phản ứng của natri hydroxide với nhôm nguyên chất. Phản ứng này tỏa nhiệt cao khi diễn ra và giải phóng nhanh chóng khí Hydro. Phản ứng này có thể được viết như sau:
- 2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
Tuy nhiên, chất được tạo thành trong dung dịch có thể chứa ion [Al(OH)4] hoặc [AlO2(H2O)2].
Phản ứng này cũng được xem như một nguồn nhiên liệu tiềm năng cho các phương tiện chạy bằng năng lượng Hydro.
Ứng dụng
Trong xử lý nước, nó được sử dụng như một phụ gia trong hệ thống làm mềm nước, như chất keo tụ để cải thiện quá trình lắng đọng, và để loại bỏ silica cũng như các hợp chất phosphat hòa tan.
Trong ngành xây dựng, natri aluminat được sử dụng để đẩy nhanh quá trình đông cứng của bê tông, đặc biệt là khi làm việc trong điều kiện lạnh giá.
Natri aluminat còn được ứng dụng trong công nghiệp giấy, sản xuất gạch chịu lửa, sản xuất alumina, và nhiều lĩnh vực khác.
Dung dịch natri aluminat là chất trung gian trong quá trình sản xuất zeolit.
- Hydroxide nhôm
Hợp chất natri | |
|---|---|
| Hợp chất vô cơ |
|
| Hợp chất hữu cơ |
|
