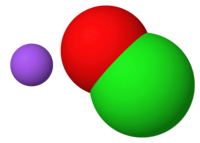
| Natri hypoclorit | |
|---|---|
Natri hypoclorit | |
| Tên khác | Natri clorat(I) |
| Nhận dạng | |
| Số CAS | 7681-52-9 |
| PubChem | 24340 |
| Số EINECS | 231-668-3 |
| Số RTECS | NH3486300 |
| Thuộc tính | |
| Công thức phân tử | NaClO |
| Khối lượng mol | 74,4411 g/mol (khan) 164,5175 g/mol (5 nước) |
| Bề ngoài | chất rắn màu trắng |
| Khối lượng riêng | 1,11 g/cm³ |
| Điểm nóng chảy | 18 °C (291 K; 64 °F) (ngậm nước, bắt đầu phân hủy thành NaCl và NaClO3 ở 40 °C) |
| Điểm sôi | 101 (phân hủy) |
| Độ hòa tan trong nước | 29,3 g/100 mL (0 °C) |
| Các nguy hiểm | |
| MSDS | ICSC 1119 (dung dịch, <10% clo hoạt động) ICSC 0482 (dung dịch, >10% clo hoạt động) |
| Phân loại của EU | Chất ăn mòn (C) Nguy hại cho môi trường (N) |
| Chỉ mục EU | 017-011-00-1 |
| NFPA 704 |
0
2
1
OX
|
| Chỉ dẫn R | R31, R34, R50 (xem Danh sách nhóm từ R) |
| Chỉ dẫn S | S1/2, S28, S45, S50, S61 (xem Danh sách nhóm từ S) |
| Các hợp chất liên quan | |
| Anion khác | Natri chloride Natri clorit Natri clorat Natri perchlorat |
| Cation khác | Lithi hypoclorit Calci hypoclorit |
| Hợp chất liên quan | Axit hypoclorơ |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa).
(cái gì ?)
Tham khảo hộp thông tin | |
Natri hypoclorit là một hợp chất hóa học với công thức NaOCl hoặc NaClO, bao gồm cation natri (Na
) và anion hypoclorit (OCl
hoặc ClO
). Hợp chất này có thể được coi là muối natri của axit hypoclorơ. Dạng khan của nó không ổn định và có thể phân hủy gây nổ, nhưng khi được kết tinh dưới dạng NaClO·5H2O, nó trở thành một chất rắn màu vàng lục nhạt, ổn định nếu được bảo quản lạnh. Dung dịch natri hypoclorit, thường có màu vàng lục nhạt, được biết đến rộng rãi như là chất tẩy trắng, và đã được sử dụng như một chất khử trùng trong các hộ gia đình từ thế kỷ 18. Các hợp chất trong dung dịch này không ổn định và dễ dàng phân hủy, giải phóng khí clo. Natri hypoclorit là chất tẩy trắng gốc clo lâu đời nhất và vẫn giữ vai trò quan trọng. Mặc dù không độc hại, nhưng do tính ăn mòn và khả năng phản ứng của nó, có thể gây nguy hiểm nếu không sử dụng đúng cách. Việc pha trộn với các sản phẩm tẩy rửa khác, như axit hoặc amonia, có thể tạo ra khí độc.
Sản xuất
Năm 1789, Claude Louis Berthollet lần đầu tiên sản xuất hypoclorit tại phòng thí nghiệm của ông ở bến cảng Javel, Paris, Pháp, bằng cách dẫn khí clo vào dung dịch natri cacbonat. Chất lỏng thu được, được gọi là 'Eau de Javel' ('nước Javel'), là một dung dịch natri hypoclorit yếu. Tuy nhiên, phương pháp này không hiệu quả và các phương pháp sản xuất thay thế đã được tìm kiếm. Phương pháp mới sử dụng vôi bị khử bằng clo (bột tẩy) và natri cacbonat để tạo ra lượng nhỏ clo. Phương pháp này thường được sử dụng để sản xuất dung dịch hypoclorit dùng làm chất khử trùng trong bệnh viện, được bán dưới các tên thương mại 'Eusol' và 'dung dịch Dakin'.
Vào cuối thế kỷ 19, E. S. Smith đã phát minh ra phương pháp chế tạo hypoclorit bằng cách thủy phân nước biển để sản xuất natri hydroxide và khí clo, sau đó kết hợp chúng để tạo ra hypoclorit. Với nguồn điện năng và nước biển rẻ, nhiều thương nhân đã tận dụng cơ hội này để đáp ứng nhu cầu thị trường về hypoclorit. Dung dịch hypoclorit đóng chai được bán dưới nhiều tên thương mại khác nhau; nhãn hiệu đầu tiên được sản xuất theo cách này là Parozone.
Hiện nay, phương pháp Hooker là một cải tiến của phương pháp trên, cho phép sản xuất natri hypoclorit quy mô công nghiệp. Theo phương pháp này, natri hypoclorit (NaClO) và natri chloride (NaCl) được tạo ra bằng cách cho khí clo vào dung dịch natri hydroxide nguội loãng. Phương pháp công nghiệp này sử dụng điện phân với một màng ngăn nhỏ giữa anốt và catôt. Dung dịch cần được giữ ở nhiệt độ dưới 40 °C nhờ các cuộn dây làm lạnh để ngăn chặn sự hình thành natri clorat không mong muốn.
- Cl2 + 2NaOH → NaCl + NaClO + H2O
Natri hydroxide và clo được sản xuất thương mại thông qua quá trình chloralkali, và không cần tách riêng chúng để điều chế natri hypoclorit.
Do đó, clo được giảm thiểu và đồng thời bị oxy hóa.
Dung dịch natri hypoclorit thương mại thường chứa một lượng đáng kể natri chloride (muối ăn) như là một sản phẩm phụ chính, như đã thấy trong phương trình trên.
Hóa học
Độ ổn định của chất rắn
Natri hypoclorit khan là một chất rắn màu trắng với cấu trúc tinh thể dạng trực thoi. Tuy nhiên, nó rất không ổn định và có thể phân hủy nổ khi tiếp xúc với nhiệt hoặc ma sát. Phản ứng phân hủy này còn bị tăng tốc bởi sự hiện diện của carbon dioxide trong không khí.
Natri hypoclorit có thể tồn tại dưới dạng tinh thể ngậm nước NaOCl·5H₂O. Dạng này ổn định hơn nhiều so với dạng khan và không có khả năng nổ. Công thức của dạng ngậm nước đôi khi được ghi là 2NaOCl·10H₂O. Natri hypoclorit pentahydrat là một chất rắn màu vàng lục nhạt, có cấu trúc tinh thể dạng trực thoi. Độ dài liên kết Cl-O trong hợp chất này là 1,686 Å. Natri hypoclorit pentahydrat nóng chảy ở nhiệt độ 25-27 °C và phân hủy nhanh chóng ở nhiệt độ phòng, do đó cần được bảo quản trong tủ lạnh. Ở nhiệt độ thấp hơn, nó khá ổn định, chỉ phân hủy 1% sau 360 ngày ở 7 °C.
Một bằng sáng chế của Mỹ năm 1966 đã mô tả phương pháp chế tạo natri hypoclorit dihydrat NaOCl·2H₂O dạng rắn với độ ổn định cao. Phương pháp này bao gồm việc loại bỏ ion clorua (Cl⁻) khỏi sản phẩm đầu ra của các quy trình sản xuất thông thường. Ion clorua được cho là tác nhân kích thích sự phân hủy của hypoclorit thành clorat (ClO₃⁻) và clorua. Trong một thử nghiệm, dihydrat được cho là chỉ phân hủy 6% sau 13,5 tháng bảo quản ở −25 °C, cho thấy dihydrat ổn định hơn nhiều so với hypoclorit dạng khan, vốn có thể phân hủy hoàn toàn trong vài ngày ở nhiệt độ phòng. Bằng sáng chế cũng cho biết dihydrat có thể được chuyển thành dạng khan bằng cách sấy chân không ở khoảng 50 °C. Chất rắn khan thu được còn có độ ổn định cao hơn, không phân hủy sau 64 giờ ở −25 °C.
Trung hòa
Sodium thiosulfate là một chất hiệu quả để trung hòa clo. Rửa tay bằng dung dịch sodium thiosulfate 5 mg/L, sau đó rửa lại bằng xà phòng và nước sẽ loại bỏ mùi clo trên tay.
Các phản ứng
Natri hypoclorit phản ứng từ từ với kim loại, chẳng hạn như kẽm, để tạo ra oxit kim loại hoặc hydroxide.
- NaClO + Zn → ZnO + NaCl
Natri hypoclorit phản ứng với axit clohydric để giải phóng khí clo:
- NaClO + 2HCl → Cl2 + H2O + NaCl
Natri hypoclorit cũng phản ứng với các axit khác như axit axetic để tạo ra axit hypoclorơ:
- NaClO + CH3COOH → HClO + CH3COONa
Khi được đun nóng hoặc bay hơi, natri hypoclorit sẽ phân hủy thành natri clorat và natri chloride:
- 3NaClO → NaClO3 + 2NaCl
Sử dụng
Chất tẩy
Dung dịch tẩy gia dụng thường chứa natri hypoclorit với nồng độ từ 3-8%. Để làm chậm sự phân hủy của natri hypoclorit thành natri chloride và natri clorat, người ta thêm natri hydroxide với nồng độ từ 0,01-0,05%.
Khử mùi
Natri hypoclorit có khả năng khử mùi hiệu quả, kết hợp với công dụng làm sạch của nó.
Trung hòa tác nhân thần kinh
Tại các cơ sở xử lý chất độc thần kinh ở Hoa Kỳ, dung dịch natri hypoclorit với nồng độ từ 0,5-2,5% được sử dụng để khử trùng thiết bị bảo hộ cá nhân (PPE) sau khi tiếp xúc với khu vực độc hại. Nó cũng được dùng để vô hiệu hóa bất kỳ sự rò rỉ ngẫu nhiên của chất độc thần kinh trong khu vực. Nồng độ natri hypoclorit thấp hơn được áp dụng trong hệ thống xử lý ô nhiễm để ngăn chặn sự xâm nhập của chất độc thần kinh vào khí thải từ lò đốt.
Giảm tổn thương da
Ngâm mình trong nước tẩy loãng có thể giúp điều trị eczema từ mức độ trung bình đến nặng. Mặc dù cơ chế hoạt động chưa được hiểu rõ, nhưng có thể là do nước tẩy có tính kháng khuẩn và chống viêm. Một nghiên cứu gần đây từ Trường Y Stanford cho thấy dung dịch natri hypoclorit rất loãng (0,005%) trong nước có thể hỗ trợ điều trị các tổn thương da gây ra bởi nhiều nguyên nhân như xạ trị, tiếp xúc quá mức với ánh nắng mặt trời và lão hóa.
Chất tẩy uế
Dung dịch loãng 1% chất tẩy gia dụng trong nước ấm được sử dụng để làm sạch các bề mặt phẳng trước khi ủ bia hoặc rượu vang. Sau khi làm sạch, bề mặt cần được rửa kỹ để tránh tạo mùi trong quá trình ủ, vì các phụ phẩm từ quá trình khử trùng bằng clo có thể gây hại.
Theo quy định của Chính phủ Mỹ (21 CFR Part 178), thiết bị chế biến thực phẩm và bề mặt tiếp xúc với thực phẩm cần được vệ sinh bằng dung dịch chứa chất tẩy trước khi tiếp xúc với thức ăn, với hàm lượng clo không vượt quá 200 phần triệu (ppm) (ví dụ: một muỗng súp chất tẩy chuẩn chứa 5,25% natri hypoclorit trong một gallon nước). Nếu nồng độ cao hơn, bề mặt cần được rửa sạch bằng nước uống sau khi vệ sinh.
Dung dịch chất tẩy gia dụng loãng (1 phần chất tẩy: 4 phần nước) hiệu quả với nhiều loại vi khuẩn và virus, và thường được dùng làm chất tẩy trùng phổ biến trong bệnh viện (đặc biệt ở Mỹ). Dung dịch này có tính ăn mòn và cần được dọn sạch sau khi sử dụng, vì vậy thường kết hợp với chất tẩy trùng bằng ethanol. Ngay cả trong các sản phẩm tẩy trùng thương mại như Virocidin-X, natri hypoclorit thường là thành phần hoạt động chính, mặc dù các sản phẩm này có thể chứa thêm chất hoạt động bề mặt (để ngăn đọng lại) và hương liệu (để che mùi thuốc tẩy).
Xử lý nước
Để khử trùng giếng hoặc hệ thống nước, người ta thường sử dụng dung dịch chất tẩy với nồng độ 3%. Đối với các hệ thống lớn hơn, natri hypoclorit là lựa chọn thực tiễn hơn vì nó có thể được sử dụng ở nồng độ thấp hơn. Tính kiềm của natri hypoclorit còn dẫn đến sự kết tủa của các khoáng chất như calci cacbonat, vì vậy quá trình khử trùng thường đi kèm với các vấn đề về cặn bẩn. Sự kết tủa này còn có thể bảo vệ vi khuẩn, làm giảm hiệu quả của phương pháp.
Natri hypoclorit đã và đang được sử dụng để khử trùng nước uống. Một dung dịch cô đặc tương đương khoảng 1 lít chất tẩy gia dụng cho 4000 lít nước được áp dụng. Liều lượng chính xác phụ thuộc vào các yếu tố như tính chất hóa học của nước, nhiệt độ, thời gian tiếp xúc, và sự hiện diện của cặn bẩn. Đối với các tình huống khẩn cấp, Cơ quan Bảo vệ Môi trường Hoa Kỳ khuyến khích sử dụng 2 mL dung dịch chất tẩy 5% cho mỗi lít nước. Nếu nước không có mùi chất tẩy, thêm 2 giọt nữa.
Mặc dù việc sử dụng các chất tẩy trùng chứa clo trong hệ thống nước gia đình rất phổ biến, nó đã dẫn đến một số tranh cãi do sự hình thành các sản phẩm phụ có hại như cloroform.
Dung dịch natri hypoclorit có tính kiềm (pH 11) được dùng để xử lý nước thải loãng chứa xyanua (< 1 g/L), chẳng hạn như nước xả từ cửa hàng mạ điện. Đối với nước thải chứa xyanua cô đặc hơn, như dung dịch mạ điện bạc xyanua, natri hypoclorit cũng được sử dụng. Quá trình xử lý được coi là hoàn tất khi phát hiện một lượng dư clo trong dung dịch.
Giải phẫu bên trong răng
Natri hypoclorit hiện đang được sử dụng trong điều trị đường tuỷ răng trong quá trình giải phẫu răng. Nó được ưa chuộng nhờ hiệu quả tiêu diệt vi sinh vật gây bệnh trong tuỷ răng. Trước đây, dung dịch Henry Drysdale Dakin 0,5% đã được sử dụng, nhưng hiện nay nồng độ sử dụng dao động từ 0,5 đến 5,25%. Ở nồng độ thấp, natri hypoclorit chủ yếu hòa tan các tế bào chết; ngược lại, ở nồng độ cao hơn, nó có thể hòa tan cả các tế bào sống, điều này không mong muốn. Tác dụng y học của nó được tăng cường khi nồng độ đạt ít nhất 1%.
Oxy hóa
Chất tẩy gia dụng, khi kết hợp với chất xúc tác chuyển pha, đã được báo cáo là có khả năng oxy hóa rượu thành các hợp chất carbonyl.
Đóng gói và bán hàng

Nước tẩy gia dụng là dung dịch natri hypoclorit với nồng độ từ 3% đến 8%. Nồng độ càng cao, hiệu quả tẩy trắng và diệt khuẩn của nước tẩy càng mạnh. Tuy nhiên, nước tẩy gia dụng có thể bị phân hủy theo thời gian, đặc biệt khi tiếp xúc với ánh sáng và nhiệt. Để kéo dài tuổi thọ của sản phẩm, thường thêm natri hydroxit vào để ổn định natri hypoclorit và làm chậm quá trình phân hủy.
Các sản phẩm tẩy rêu đen cho sân vườn thường là dung dịch natri hypoclorit với nồng độ khoảng 10%. Chúng có nhiều tên gọi khác nhau tùy theo nhà sản xuất, như nước tẩy, Hypo, Everchlor, Chloros, Hispec, Bridos, Bleacol, hoặc Vo-redox 9110.
Natri hypoclorit là một chất khử trùng hiệu quả, được dùng rộng rãi trong nhiều ứng dụng, bao gồm khử trùng nước. Trong hệ thống cấp nước, dung dịch natri hypoclorit 12% thường được sử dụng, còn ở các nhà máy xử lý nước thải, dung dịch 15% là phổ biến hơn. Đối với khử trùng nước uống tại điểm sử dụng, liều lượng thường từ 0,2 đến 2 mg natri hypoclorit trên một lít nước.
Dung dịch loãng natri hypoclorit (từ 50 ppm đến 1,5%) có mặt trong các bình xịt khử trùng và khăn lau dùng cho bề mặt cứng.
Tác động môi trường
Dung dịch natri hypoclorit có hiệu quả diệt khuẩn cao, nhưng ảnh hưởng của nó đối với môi trường khá hạn chế. Điều này là do ion hypochlorite, thành phần chủ yếu của dung dịch, phân hủy nhanh chóng trước khi kịp được sinh vật hấp thụ.
Dù là chất tẩy rửa phổ biến, natri hypoclorit có thể tạo ra các hợp chất hữu cơ chứa clo, trong đó một số là chất gây ung thư. Những hợp chất này có thể hình thành trong quá trình bảo quản, sử dụng gia đình và công nghiệp. Ví dụ, khi pha trộn thuốc tẩy với nước thải, 1-2% clo có thể tạo ra các hợp chất hữu cơ. Đến năm 1994, không phải tất cả các sản phẩm phụ đều được xác định, nhưng những hợp chất đã được biết đến bao gồm chloroform và carbon tetrachloride. Mức độ tiếp xúc với những hóa chất này khi sử dụng được đánh giá là nằm trong giới hạn phơi nhiễm nghề nghiệp.
An toàn
Natri hypoclorit là một chất oxy hóa mạnh và sản phẩm của phản ứng oxy hóa này có tính ăn mòn. Dung dịch này có thể gây bỏng da và tổn hại mắt, đặc biệt khi ở nồng độ cao. Tuy nhiên, theo tiêu chuẩn của NFPA, chỉ những dung dịch natri hypoclorit có nồng độ từ 40% trở lên mới được coi là chất oxy hóa nguy hiểm. Các dung dịch có nồng độ dưới 40% được xếp vào nhóm oxy hóa có mức độ nguy hiểm trung bình (NFPA 430, 2000).
Khi khử trùng nước uống bằng clo, có thể hình thành các chất hữu cơ nguy hiểm như trihalogenomethan (hay còn gọi là halogenoform), một chất gây ung thư.
Chất tẩy gia dụng và dung dịch khử trùng hồ bơi thường chứa một lượng kiềm đáng kể (như xút ăn da, NaOH) trong quá trình sản xuất. Tiếp xúc với da có thể gây kích ứng hoặc bỏng do việc loại bỏ mỡ và xà phòng trên da cùng với sự phá hủy tế bào. Cảm giác trơn trên da là kết quả của quá trình này.
Natri thiosunfat (còn gọi là hypo) là chất trung hòa clo hiệu quả. Rửa tay bằng dung dịch natri thiosunfat nồng độ 5 mg/L, sau đó giặt lại với xà phòng và nước, sẽ loại bỏ nhanh chóng dấu vết của clo trên tay.
Khi kết hợp chất tẩy với một số chất tẩy gia dụng khác, có thể xảy ra những phản ứng nguy hiểm. Ví dụ, trộn chất tẩy axit với natri hypoclorit sẽ tạo ra khí clo, trong khi trộn với dung dịch amonia (bao gồm nước tiểu) sẽ tạo ra cloramin.
- NH4OH + NaOCl → NaOH + NH2Cl + H2O
Cả khí clo và khí cloramin đều có tính độc hại. Chất tẩy có thể phản ứng mạnh mẽ với oxy già và sinh ra khí oxy.
- H2O2 + NaOCl → NaCl + H2O + O2
Theo thống kê, mỗi năm ở Anh có khoảng 3300 vụ tai nạn liên quan đến natri hypoclorit cần sự can thiệp y tế (RoSPA, 2002).
Một nghiên cứu toàn châu Âu gần đây cho thấy natri hypoclorit và các hợp chất hữu cơ khác (như chất hoạt động bề mặt và chất tạo hương) trong sản phẩm tẩy rửa gia dụng có thể phản ứng với nhau, tạo ra các hợp chất chứa clo dễ bay hơi (VOCs). Những hợp chất này phát tán trong suốt quá trình tẩy rửa, nhiều trong số đó là độc hại và có khả năng gây ung thư. Nghiên cứu còn chỉ ra rằng nồng độ không khí trong nhà tăng đáng kể (từ 8 đến 52 lần cloroform và 1 đến 1170 lần cacbon tetrachloride, vượt mức cho phép) khi sử dụng các sản phẩm chứa chất tẩy. Sự gia tăng nồng độ VOCs trong không khí trong nhà thấp nhất với chất tẩy thông thường và cao nhất với loại 'chất lỏng đặc và gel'. Sự gia tăng đáng kể các hợp chất VOCs trong không khí trong nhà (như cacbon tetrachloride và cloroform) cho thấy việc sử dụng chất tẩy có thể là nguồn gây ra phơi nhiễm quan trọng. Mặc dù các tác giả cảnh báo rằng việc sử dụng các sản phẩm này có thể tăng nguy cơ ung thư, kết luận vẫn còn đang trong giai đoạn giả thuyết.
- Mức độ cao nhất của cacbon tetrachloride (được coi là nguy hiểm nhất) là 459 μg/m³, tương đương 0,073 ppm (phần triệu) hoặc 73 ppb (phần tỉ). OSHA cho phép nồng độ trung bình trong 8 giờ là 10 ppm, cao hơn khoảng 140 lần so với mức cho phép.
- Mức nồng độ tối đa được OSHA cho phép (phơi nhiễm trong 5 phút từ 4 giờ) là 220 ppm, gấp đôi mức cao nhất được ghi nhận (khoảng cách thêm từ một chai chất tẩy mẫu).
Các nghiên cứu tiếp theo về việc sử dụng các sản phẩm này và các lộ trình khác có thể làm phát sinh thêm các vấn đề khác. Dù các tác giả đề cập đến việc các khí này có thể gây hại cho tầng ôzôn và hiệu ứng nhà kính, lượng khí tạo ra chỉ rất ít, theo quy định, nên ảnh hưởng từ các nguồn khác cần được giảm thiểu.
Giới hạn trong lĩnh vực chăm sóc sức khỏe
Vào tháng 10 năm 2008, Viện Nghiên cứu Y tế và Chăm sóc Quốc gia Anh (NICE) đã khuyến cáo không nên sử dụng dung dịch Dakin trong chăm sóc vết thương thông thường.
Ghi chú
- Jones, F.-L. (1972). “Ngộ độc clo do trộn lẫn các chất tẩy gia dụng”. J. Am. Med. Assoc. 222: 1312. doi:10.1001/jama.222.10.1312.
- Institut National de Recherche et de Sécurité. (2004). 'Nước và dung dịch tẩy trắng. Natri hypoclorit trong dung dịch'. Fiche toxicologique n° 157, Paris.
Các liên kết bên ngoài
- International Chemical Safety Card 0482 (dung dịch < 10% clo hoạt động)
- International Chemical Safety Card 1119 (dung dịch >10% clo hoạt động)
- European Chemicals Bureau Lưu trữ ngày 22 tháng 7 năm 2011 tại Wayback Machine
- Institut national de recherche et de sécurité Lưu trữ ngày 28 tháng 4 năm 2010 tại Wayback Machine (trong tiếng Pháp)
- Home and Leisure Accident Statistics 2002 Lưu trữ ngày 12 tháng 1 năm 2006 tại Wayback Machine (UK RoSPA)
- Emergency Disinfection of Drinking Water (Cơ quan Bảo vệ Môi trường Hoa Kỳ)
- Chlorinated Drinking Water Lưu trữ ngày 12 tháng 10 năm 2005 tại Wayback Machine (IARC Monograph)
- NTP Study Report TR-392: Chlorinated & Chloraminated Water (US NIH)
- Guidelines for the Use of Chlorine Bleach as a Sanitizer in Food Processing Operations Lưu trữ ngày 28 tháng 5 năm 2008 tại Wayback Machine (Trường Đại học Oklahoma State)
Chất tẩy trùng và chất tẩy uế (D08) |
|---|
Hợp chất natri | |
|---|---|
| Hợp chất vô cơ |
|
| Hợp chất hữu cơ |
|
Hợp chất chlor |
|---|
