
| Natri thiosulfat | |
|---|---|
Natri thiosulfat | |
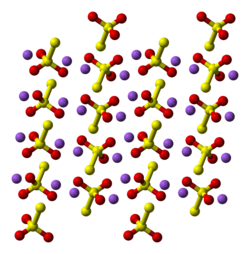
Cấu trúc tinh thể của phân tử natri thiosulfat ngậm 5 nước | |
| Danh pháp IUPAC | Natri thiosulfat |
| Tên khác | Natri hyposulfit |
| Nhận dạng | |
| Số CAS | 7772-98-7 |
| PubChem | 24477 |
| ChEMBL | 1201157 |
| Số RTECS | XN6476000 |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ |
| InChI | đầy đủ |
| UNII | L0IYT1O31N |
| Thuộc tính | |
| Công thức phân tử | Na2S2O3 |
| Khối lượng mol | 158.11 g/mol |
| Bề ngoài | tinh thể màu trắng |
| Mùi | không mùi |
| Khối lượng riêng | 1.667 g/cm³ |
| Điểm nóng chảy | 48.3 °C (ngậm 5 nước) |
| Điểm sôi | 100 °C (ngậm 5 nước, - 5H2O phân hủy) |
| Độ hòa tan trong nước | 76.4 g/100 g H20(20 °C) |
| Cấu trúc | |
| Các nguy hiểm | |
| MSDS | External MSDS |
| Chỉ mục EU | không có trong danh sách |
| NFPA 704 |
0
1
0
|
| Điểm bắt lửa | không cháy |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa).
(cái gì ?)
Tham khảo hộp thông tin | |
Natri Thiosulfat (Na2S2O3) là một hợp chất tinh thể không màu, thường xuất hiện dưới dạng muối ngậm 5 phân tử nước, Na2S2O3•5H2O. Chất này còn được gọi là natri hyposulfit hoặc đơn giản là 'hypo'.
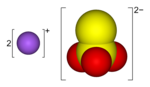
Anion thiosulfat có cấu trúc tứ diện và được hình thành từ việc thay thế một nguyên tử oxy trong anion sulfat bằng một nguyên tử lưu huỳnh. Liên kết S-S là liên kết đơn, cho thấy lưu huỳnh có điện tích âm đáng kể và sự tương tác S-O có đặc điểm của một liên kết đôi. Proton hóa ion thiosulfat lần đầu tiên xảy ra ở lưu huỳnh.
Ứng dụng trong công nghiệp và tổng hợp phòng thí nghiệm
Trong công nghiệp, natri thiosulfat chủ yếu được tạo ra từ các sản phẩm phụ của quá trình sản xuất natri sulfide hoặc thuốc nhuộm lưu huỳnh. Ở phòng thí nghiệm, muối này có thể được tổng hợp bằng cách phản ứng giữa natri sulfit và lưu huỳnh khi đun nóng.
Các phản ứng chủ yếu và ứng dụng của chúng
Anion thiosulfat phản ứng đặc hiệu với các acid loãng để sinh ra lưu huỳnh, lưu huỳnh dioxide và nước:
- Na2S2O3 + 2 HCl → 2 NaCl + S + SO2 + H2O
Phản ứng này còn được gọi là 'phản ứng chuẩn độ', vì khi lưu huỳnh đạt đến nồng độ nhất định, dung dịch sẽ chuyển từ không màu sang vàng nhạt. Phản ứng này đang được ứng dụng để sản xuất lưu huỳnh dạng keo. Khi proton hóa ở nhiệt độ thấp, H2S2O3 (acid thiosulfuric) được hình thành, đây là một acid có độ mạnh tương đối với pKas khoảng 0.6 và 1.7 cho sự phân ly lần lượt H.
Phép chuẩn độ iod
Trong hóa học phân tích, phản ứng quan trọng nhất của anion thiosulfat là phản ứng định lượng với iod, chuyển iod thành ion iođua và chính nó bị oxy hóa thành ion tetrathionat:
- 2 S2O3(aq) + I2(aq) → S4O6(aq) + 2 I(aq)
Nhờ vào bản chất định lượng của phản ứng và thời hạn sử dụng lâu dài của Na2S2O3•5H2O, nó thường được dùng làm chất chuẩn trong phép chuẩn độ iod.
Ứng dụng quan trọng này có thể được thực hiện để đo lượng oxy trong nước qua một chuỗi phản ứng phức tạp, cũng như để đánh giá nồng độ thể tích của dung dịch và xác định hàm lượng clo trong nước và bột tẩy.
Trong xử lý ảnh
Nguyên tử lưu huỳnh ở bậc bốn trong S2O3 có khả năng kết hợp với các kim loại mềm nhờ ái lực mạnh mẽ của nó. Vì vậy, các muối bạc halide như AgBr, thành phần chính của chất nhũ ảnh, sẽ hòa tan khi tiếp xúc với dung dịch thiosulfat:
- 2 S2O3 + AgBr → [Ag(S2O3)2] + Br
Trong ứng dụng cho xử lý ảnh, phát hiện bởi John Herschel và được sử dụng cho cả phim và giấy ảnh, natri thiosulfat được gọi là chất xử lý ảnh, hay còn được biết đến với tên gọi hypo, xuất phát từ tên cũ của nó là natri hyposulfit.
Tinh chế vàng
Natri thiosulfat là thành phần chính của một chất ngâm chiết thay thế cyanide trong việc tách vàng. Nó tạo ra một phức chất ổn định với ion vàng(I), [Au(S2O3)2]. Phương pháp này có ưu điểm là thiosulfat không độc và có thể xử lý các quặng chịu nhiệt trong quá trình cyanide (như carbon hay quặng Carlin). Tuy nhiên, phương pháp này vẫn gặp khó khăn với việc tiêu hao thiosulfat cao và thiếu công nghệ tái tạo hợp lý vì [Au(S2O3)2] không được hấp thụ bởi than hoạt tính, một công nghệ chính trong quá trình cyanide để tách phức vàng khỏi hồ quặng.
Hóa học phân tích
Natri thiosulfat cũng được ứng dụng trong hóa phân tích. Khi đun nóng mẫu thử có chứa cation nhôm, nó sẽ tạo ra một kết tủa màu trắng đặc trưng:
- 2 Al + 3 S2O3 + 3 H2O → 3 SO2 + 3 S + 2 Al(OH)3
Y khoa
- Nó được sử dụng như một chất giải độc cho cyanide, hoạt động bằng cách cung cấp lưu huỳnh để chuyển cyanide thành thioxyanat, sau đó thải ra ngoài qua nước tiểu nhờ enzim rhodanase.
- Nó cũng được dùng trong điều trị phản vệ calci trong thẩm tách máu cho bệnh nhân suy thận mãn tính giai đoạn cuối.
- Trong hóa trị liệu, natri thiosulfat giúp ngăn ngừa sự ankyl hóa và bảo vệ mô bằng cách cung cấp chất nền cho tác nhân ankyl hóa phân bố đều qua các mô dưới da. Liều thường dùng là 2mL dung dịch 0.17M (4mL natri thiosulfat 10% hòa với 6mL nước vô trùng). Có thể tiêm dưới da ở nhiều vị trí với một ống tiêm nhỏ. Dữ liệu về phương pháp này còn hạn chế và có một số khuyến cáo cần lưu ý.
- Nó được sử dụng trong việc tắm đứng để điều trị bệnh ecpet mảng tròn và là một chất diệt nấm hiệu quả cho chứng đốm nấm lông.
- Thiosulfat còn được dùng để đo thể tích dịch ngoại bào và đánh giá tỉ lệ lọc của cầu thận.
Các ứng dụng khác
Natri thiosulfat còn được sử dụng trong các lĩnh vực sau:
- Được dùng làm thành phần trong các sản phẩm sưởi tay và túi nhiệt, nhờ vào quá trình kết tinh tỏa nhiệt của dung dịch siêu lạnh.
- Chất tẩy rửa
- Đo pH của chất tẩy: Các chất chỉ thị và chỉ thị pH dạng lỏng thường bị hủy bởi chất tẩy. Tuy nhiên, khi thêm natri thiosulfat vào dung dịch, nó sẽ trung hòa tác dụng tẩy của chất tẩy, cho phép các chất chỉ thị đo pH của dung dịch tẩy. Phản ứng này tương tự như phản ứng với iod, với thiosulfat khử hypoclorit thành sulfat. Phương trình phản ứng như sau:
- 4 NaClO + Na2S2O3 + 2 NaOH → 4 NaCl + 2 Na2SO4 + H2O
- Khử clo trong nước bể cá hoặc xử lý nước thải từ quá trình xử lý nước thải đầu tiên để xả ra môi trường. Phản ứng này tương tự như phản ứng khử iod. Để xử lý nước bể cá, cần khoảng 0.1 đến 0.3 gram natri thiosulfat cho 10 lít nước.
- Giảm nồng độ clo trong hồ bơi hoặc bể nước nóng sau khi tiến hành clo hóa.
- Được dùng để tẩy màu iod, chẳng hạn như sau khi thực hiện phản ứng với nitơ triiođua.
- Tương tự, natri thiosulfat phản ứng với brom để tạo ra các sản phẩm không độc hại. Dung dịch natri thiosulfat thường được sử dụng để phòng ngừa trong phòng thí nghiệm sau khi làm việc với brom.
- Đánh giá chất lượng nước trong các nghiên cứu vi khuẩn học.
- Ứng dụng trong ngành thuộc da.
- Được sử dụng để chứng minh khái niệm tốc độ phản ứng trong môn hóa học. Ion thiosulfat có thể phân hủy thành ion sulfit và tạo ra huyền phù lưu huỳnh dạng keo mờ. Phương trình phản ứng acid-catalyzed là:
- S2O3(d) → SO3(d) + S(s)
- Được sử dụng để chứng minh khái niệm siêu lạnh trong vật lý. Natri thiosulfat có thể dễ dàng làm quá lạnh ở nhiệt độ phòng, và khi tinh thể hình thành, bạn có thể cảm nhận được sự tăng nhiệt độ lên đến 48,3 °C.
- Được ứng dụng trong công thức gỉ đồng cho các hợp kim đồng.
- Được sử dụng trong điều chế dược phẩm như một chất hoạt động bề mặt anion để cải thiện sự phân tán.
- Thú vị khi dùng trong các thí nghiệm để tạo dung dịch quá bão hòa.
