
| Đồng(I) oxide | |
|---|---|
Mẫu đồng(I) oxide | |
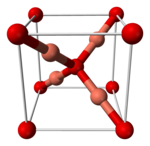
Cấu trúc của đồng(I) oxide | |
| Danh pháp IUPAC | Copper(I) oxide |
| Tên khác | Đicopper oxide Cuprơ oxide Cuprit Oxide đồng đỏ Cuprum(I) oxide Đicuprum oxide |
| Nhận dạng | |
| Số CAS | 1317-39-1 |
| PubChem | 10313194 |
| Số EINECS | 215-270-7 |
| KEGG | C18714 |
| ChEBI | 81908 |
| Số RTECS | GL8050000 |
| Ảnh Jmol-3D | ảnh ảnh 2 |
| SMILES | đầy đủ |
| InChI | đầy đủ |
| ChemSpider | 8488659 |
| UNII | T8BEA5064F |
| Thuộc tính | |
| Công thức phân tử | Cu2O |
| Khối lượng mol | 143,0914 g/mol |
| Bề ngoài | Màu đỏ nâu – rắn |
| Khối lượng riêng | 6 g/cm³, rắn |
| Điểm nóng chảy | 1.235 °C (1.508 K; 2.255 °F) |
| Điểm sôi | |
| Độ hòa tan trong nước | Không tan |
| Cấu trúc | |
| Cấu trúc tinh thể | lập phương |
| Các nguy hiểm | |
| MSDS | ScienceLab.com |
| Phân loại của EU | Độc hại (Xn) Nguy hiểm cho môi trường (N) |
| Chỉ mục EU | 029-002-00-X |
| Chỉ dẫn R | R22, R50/53 |
| Chỉ dẫn S | S2, S22, S60, S61 |
| Các hợp chất liên quan | |
| Anion khác | Đồng(I) sulfide Đồng(I) selenide Đồng(I) teluride |
| Cation khác | Đồng(II) oxide Bạc(I) oxide Niken(II) oxide Kẽm oxide |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). Tham khảo hộp thông tin | |
Oxít Đồng(I) (công thức hóa học: Cu2O) là một loại hợp chất oxit của đồng. Nó có khối lượng phân tử là 144 g/mol, nhiệt độ nóng chảy là 1230°C.
Chất này thường tồn tại tự nhiên dưới dạng bột màu đỏ. Nó cũng có thể được tạo ra từ oxit đồng(II) thông qua phản ứng hóa học trong môi trường nhiệt độ cao, CuO chuyển thành Cu2O màu đỏ sáng:
- 2CuO + CO → Cu2O + CO2
Các tính chất hóa học
Tương tự như oxit đồng(II), oxit đồng(I) cũng có các tính chất hóa học tương đương.
- Tác dụng với axit tạo thành muối và nước:
- Cu2O + 2HCl → 2CuCl + H2O
- Tác dụng với oxit axit tạo thành muối:
- 3Cu2O + P2O5 → 2Cu3PO4
- Bị tác động bởi các chất khử ở nhiệt độ cao:
- Cu2O + 2K → K2O + 2Cu
- Cu2O + H2 → H2O + 2Cu
Các đặc tính khác
- Tác dụng với oxi tạo thành oxit đồng(II):
- 2Cu2O + O2 → 4CuO
- Tác dụng với các chất oxy hóa mạnh để hình thành oxit đồng(II).
Các ứng dụng
Trong lĩnh vực vật liệu gốm sứ
Đồng(I) oxit được sử dụng để tạo màu sắc cho men gốm. Để có màu đỏ sáng, chỉ cần dùng một lượng rất nhỏ đồng(I) oxit (0,5%). Nếu lượng đồng cao hơn, có thể tạo ra các hạt đồng kim loại nhỏ trong men nung gây nên màu đỏ máu bò.
Khi có sự có mặt của bari trong men làm cho đồng đỏ, màu sắc sẽ chuyển thành tím. Trong men đồng đỏ, sử dụng nhiều khoáng chất như thạch thạch và thêm oxit bari để tạo ra các gam màu từ ngọc lam đến xanh thẫm, phụ thuộc vào lượng đồng(I) oxit có trong đó. Fluorua khi được sử dụng cùng đồng oxit sẽ cho màu xanh lục.
Trong lĩnh vực vật liệu điện,
Đồng(I) oxit là một loại chất bán dẫn. Đôi khi cặp Cu2O-Cu chỉ cho phép dòng điện từ đồng sang đồng(I) oxit, với lớp Cu2O đóng vai trò bán dẫn loại n và lớp đồng đóng vai trò là bán dẫn loại p. Với tính chất bán dẫn, đồng(I) oxit được sử dụng rộng rãi trong việc sản xuất pin mặt trời và giáo dục.
Quá trình sản xuất
- Sử dụng khí CO để khử CuO ở nhiệt độ cao:
- 2CuO + CO → Cu2O + CO2
- Đốt đồng trong môi trường thiếu oxi:
- 4Cu + O2 → 2Cu2O
- Điện phân anot đồng trong dung dịch NaCl dưới môi trường kiềm.
- Đồng(II) oxit

Hợp chất đồng |
|---|
- Cổng thông tin Hóa học
Oxide |
|---|
