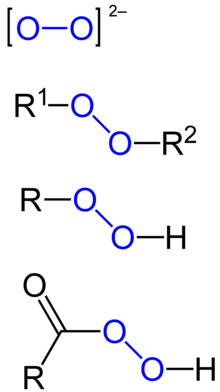
Peroxit là hợp chất có cấu trúc R-O-O-R. Nhóm O-O trong peroxit được gọi là nhóm peroxit hoặc nhóm peroxo. Trái với các ion oxit, các nguyên tử oxy trong ion peroxit có trạng thái oxy hóa là -1.
Peroxit ổn định nhất là hydroperoxit. Nó được bán dưới dạng dung dịch nước với nhiều nồng độ khác nhau. Hydroperoxit là chất lỏng trong suốt có màu lam nhạt nhưng các dung dịch nước của nó lại không có màu. Nó chủ yếu được sử dụng làm chất oxy hóa và chất tẩy trắng. Tuy nhiên, hydroperoxit cũng được tổng hợp trong cơ thể người thông qua các enzym oxidase. Các dung dịch đặc có thể gây nguy hiểm khi tiếp xúc với các hợp chất hữu cơ.
Ngoài hydroperoxit, còn có một số loại peroxit chính như:
- Acid peroxy, các dẫn xuất peroxy của nhiều axit thông thường, như acid peroxymonosulfuric và acid peracetic.
- Peroxit kim loại, như bari peroxit (BaO2) và natri peroxit (Na2O2).
- Peroxit hữu cơ, các hợp chất có công thức R1-O-O-R2. Ví dụ như tert-butylhydroperoxit
- Peroxit nhóm chính, các hợp chất với liên kết E-O-O-E (E = nguyên tố nhóm chính), ví dụ như kali peroxydisulfat (K2S2O8).
Các hợp chất peroxit có thể được phân loại thành hữu cơ và vô cơ. Trong khi các peroxit vô cơ có tính chất ion, muối, các peroxit hữu cơ bị chi phối bởi các liên kết đồng hóa trị. Liên kết hóa học O-O của peroxit không ổn định và dễ dàng phân chia thành các gốc phản ứng thông qua sự phân ly homolytic. Vì vậy, peroxit tự nhiên chỉ tồn tại với số lượng nhỏ, trong nước, khí quyển, thực vật và động vật. Sự hình thành ion peroxit đã được nhấn mạnh là một trong những cơ chế chính để các oxit chứa oxy dư thừa trong tinh thể ion và có thể ảnh hưởng lớn đến nhiều ứng dụng công nghiệp bao gồm cả pin nhiên liệu rắn.
Peroxit có khả năng làm trắng các chất hữu cơ và do đó được sử dụng trong một số sản phẩm tẩy rửa và làm đẹp tóc. Các ứng dụng lớn khác bao gồm y học và công nghiệp hóa chất, trong đó peroxit được dùng trong các phản ứng tổng hợp khác nhau hoặc là sản phẩm trung gian. Với sản lượng hàng năm lên đến 2 triệu tấn, hydroperoxit là loại peroxit quan trọng nhất về mặt kinh tế. Nhiều peroxit là các chất nguy hiểm và không ổn định; chúng không thể được lưu trữ lâu dài và do đó phải được tổng hợp và sử dụng ngay.
Các superoxit, dioxygenyl, ozon và ozonit được xem xét riêng.
- Cổng thông tin Hóa học
Các nhóm chức | |
|---|---|
Lớp hóa học: Rượu • Aldehyde • Alkan • Alken • Alkyl • Alkadien • Hydrocarbon thơm • Amid • Amin • Azo • Dẫn xuất benzen • Acid carboxylic • Cumulen • Cyanat • Disulfide • Este • Ether • Haloalkan • Hydrazon • Imin • Isocyanide • Isocyanat • Keton • Oxim • Nitril • Nitro • Nitroso • Peroxide • Acid phosphoric • Dẫn xuất pyridin • Sulfon • Acid sulfonic • Sulfoxide • Thioeste • Thioether • Thiol • Methylen • Methyl • Methin • Methyliden |
| Tiêu đề chuẩn |
|
|---|
