Vào ngày 26 tháng 11, Tổ chức Y tế Thế giới đã chỉ định chủng virus corona tăng cao ở Nam Phi là một “biến thể đáng lo ngại” và đặt tên nó là Omicron. Ngày hôm sau, giáo sư Sriram Subramaniam của Đại học British Columbia tải xuống một chuỗi gen được đăng trực tuyến và đặt hàng mẫu gen Omicron để được gửi đến phòng thí nghiệm của ông.
Nhóm của Subramaniam sử dụng kính hiển vi điện tử để tiết lộ cấu trúc 3D của các protein, nhằm hiểu rõ hơn cách chúng hoạt động. Họ đã từng ánh xạ các protein gai mà virus corona sử dụng để kết hợp và xâm nhập vào tế bào người đối với một số chủng virus trước đó. Việc mô tả protein gai của Omicron cảm thấy gấp gáp vì gen của nó khác biệt theo những cách có thể giải thích sự lan truyền nhanh chóng của biến thể này. Nhưng giống như những người mua sắm trực tuyến vào cuối tuần đó, Subramaniam phải kiên nhẫn: Cho đến khi các mẫu đến qua đường bưu điện, ông không thể đặt protein Omicron dưới kính hiển vi.
Ở một phần của lục địa khác, nhà nghiên cứu genôm tính toán Colby Ford từ Đại học North Carolina tại Charlotte cũng đã nghĩ về protein gai của Omicron. Người thân của ông đã hỏi ông một câu hỏi cũng làm phiền nhiều chuyên gia: Liệu Omicron có tránh được các loại vắc xin hiện tại? Những loại vắc xin đó dạy cơ thể phản ứng với protein gai từ một chủng virus trước đó. Thay vì đặt hàng vật tư thí nghiệm, Ford đã thử một con đường tắt vừa được phát minh gần đây. Cùng ngày WHO đặt tên cho Omicron, ông đã sử dụng phần mềm trí tuệ nhân tạo miễn phí để dự đoán cấu trúc từ chuỗi axit amin được mã hóa trong gen của Omicron.
Chưa đầy một giờ sau đó, Ford đã nhận được kết quả đầu tiên của mình và nhanh chóng đăng chúng trực tuyến. Đầu tháng Mười Hai, ông và hai đồng nghiệp đăng một bản báo cáo chi tiết hơn, hiện đã được chấp nhận xuất bản, bao gồm dự đoán rằng một số kháng thể đối với các chủng trước đó sẽ ít hiệu quả hơn đối với Omicron.
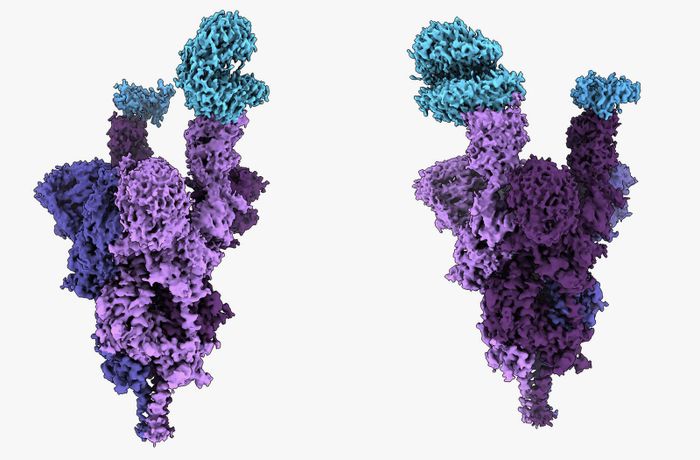
Phòng thí nghiệm của Subramaniam sớm nhận được các mẫu gen Omicron và công bố các quan sát qua kính hiển vi về cấu trúc cùng với kết quả từ các thử nghiệm kháng thể thực tế vào ngày 21 tháng Mười Hai. Một trong hai cấu trúc dự đoán của Ford đã chứng minh khá chính xác: Ông tính toán rằng các vị trí của các nguyên tử trung tâm khác nhau khoảng một nửa angstrom, xấp xỉ bán kính của một nguyên tử hydro. “Những công cụ này cho phép bạn đưa ra dự đoán có căn cứ rất nhanh chóng—điều quan trọng trong tình huống như Covid,” Ford nói. “Với bất kỳ virus mới nào xuất hiện, người khác sẽ lặp lại những gì tôi đã làm ở đây.”
Cách dự đoán vượt trội trước các thí nghiệm về protein gai của Omicron phản ánh một sự thay đổi lớn gần đây trong sinh học phân tử do Trí tuệ Nhân tạo mang lại. Phần mềm đầu tiên có khả năng dự đoán chính xác cấu trúc protein trở nên phổ biến chỉ vài tháng trước khi Omicron xuất hiện, nhờ vào các nhóm nghiên cứu cạnh tranh tại phòng thí nghiệm Trí tuệ Nhân tạo DeepMind thuộc Alphabet tại Anh và Đại học Washington.
Ford sử dụng cả hai gói phần mềm, nhưng do cả hai đều không được thiết kế hoặc xác minh để dự đoán các biến đổi nhỏ do đột biến như của Omicron, kết quả của ông chỉ là gợi ý hơn là cuối cùng. Một số nhà nghiên cứu đã xem xét chúng với sự nghi ngờ. Nhưng thực tế là ông có thể dễ dàng thử nghiệm với Trí tuệ Nhân tạo dự đoán protein mạnh mẽ là minh chứng cho việc những đột phá gần đây đang thay đổi cách mà các nhà sinh học làm việc và suy nghĩ.
Subramaniam cho biết ông nhận được bốn hoặc năm email từ những người đề xuất cấu trúc gai Omicron dự đoán trong khi ông đang làm việc để đạt được kết quả phòng thí nghiệm của mình. “Khá nhiều người làm điều này chỉ vì vui,” ông nói. Đo lường trực tiếp cấu trúc protein sẽ tiếp tục là thước đo cuối cùng, Subramaniam nói, nhưng ông mong đợi dự đoán Trí tuệ Nhân tạo sẽ ngày càng trở nên quan trọng hơn trong nghiên cứu—kể cả trong các đợt bùng phát dịch bệnh trong tương lai. “Nó thay đổi,” ông nói.
Do hình dạng của một protein xác định cách nó hoạt động, việc biết cấu trúc của nó có thể hỗ trợ mọi loại nghiên cứu sinh học, từ các nghiên cứu về tiến hóa đến công việc về bệnh tật. Trong nghiên cứu dược phẩm, việc xác định cấu trúc protein có thể giúp phát hiện các mục tiêu tiềm năng cho các liệu pháp mới.
Xác định cấu trúc của một protein không hề đơn giản. Chúng là những phân tử phức tạp được lắp ráp từ hướng dẫn được mã hóa trong gen của một cơ thể để phục vụ như enzyme, kháng thể và nhiều thiết bị khác của cuộc sống. Protein được tạo ra từ chuỗi các phân tử gọi là axit amin có thể gập lại thành các hình dạng phức tạp có cách hoạt động khác nhau.
Giải mã cấu trúc của một protein truyền thống thường liên quan đến công việc kỹ lưỡng trong phòng thí nghiệm. Hầu hết trong số khoảng 200.000 cấu trúc được biết đến đã được ánh xạ bằng cách sử dụng một quá trình phức tạp trong đó protein được tạo thành thành tinh thể và bị tia X đập vào. Các kỹ thuật mới như kính hiển vi điện tử được sử dụng bởi Subramaniam có thể nhanh hơn, nhưng quá trình vẫn chưa dễ dàng.
Cuối năm 2020, hy vọng lâu dài rằng máy tính có thể dự đoán cấu trúc protein từ chuỗi axit amin đột nhiên trở thành hiện thực, sau nhiều thập kỷ tiến triển chậm rãi. Phần mềm AlphaFold của DeepMind chứng minh được độ chính xác cao đến mức đoạt giải trong cuộc thi dự đoán protein, khiến cho John Moult, một trong những người sáng lập thử thách và là giáo sư tại Đại học Maryland, tuyên bố vấn đề đã được giải quyết. “Sau khi làm việc cá nhân trên vấn đề này trong thời gian dài,” Moult nói, thành tựu của DeepMind là “một khoảnh khắc rất đặc biệt.”
Khoảnh khắc cũng làm cho một số nhà khoa học cảm thấy bực bội: DeepMind không ngay lập tức công bố chi tiết về cách AlphaFold hoạt động. “Bạn đang ở trong tình huống kỳ lạ khi có một bước tiến lớn trong lĩnh vực của bạn, nhưng bạn không thể xây dựng trên nó,” David Baker, người điều hành phòng thí nghiệm tại Đại học Washington nghiên cứu về dự đoán cấu trúc protein, nói với Mytour năm trước. Nhóm nghiên cứu của ông đã sử dụng gợi ý từ DeepMind để hướng dẫn thiết kế phần mềm mã nguồn mở gọi là RoseTTAFold, ra mắt vào tháng Sáu, tương tự nhưng không mạnh mẽ như AlphaFold. Cả hai dựa trên thuật toán học máy được điều chỉnh để dự đoán cấu trúc protein bằng cách huấn luyện trên một bộ sưu tập hơn 100.000 cấu trúc được biết đến. Tháng sau đó, DeepMind công bố chi tiết về công việc của họ và phát hành AlphaFold để ai cũng có thể sử dụng. Bất ngờ, thế giới có hai cách để dự đoán cấu trúc protein.
Minkyung Baek, một nghiên cứu viên sau tiến sĩ trong phòng thí nghiệm của Baker, người đứng đầu công việc trên RoseTTAFold, nói cô đã bất ngờ trước tốc độ nhanh chóng mà việc dự đoán cấu trúc protein đã trở thành tiêu chuẩn trong nghiên cứu sinh học. Google Scholar báo cáo rằng các bài báo của Đại học Washington và DeepMind về phần mềm của họ đã được trích dẫn bởi hơn 1.200 bài báo học thuật trong thời gian ngắn kể từ khi chúng xuất hiện.
Mặc dù các dự đoán chưa chứng minh được tính quyết định trong công việc về Covid-19, cô tin rằng chúng sẽ trở nên ngày càng quan trọng đối với phản ứng với các bệnh tương lai. Câu trả lời chấm dứt đại dịch sẽ không tự nảy ra từ thuật toán, nhưng cấu trúc dự đoán có thể giúp các nhà khoa học xây dựng chiến lược. “Một cấu trúc dự đoán có thể giúp bạn tập trung nỗ lực thực nghiệm vào những vấn đề quan trọng nhất,” Baek nói. Cô đang cố gắng để RoseTTAFold có thể dự đoán chính xác cấu trúc của kháng thể và các protein xâm nhập khi kết hợp với nhau, điều này sẽ làm cho phần mềm hữu ích hơn đối với các dự án về bệnh truyền nhiễm.
Mặc dù hiệu suất ấn tượng, các dự đoán về protein không tiết lộ mọi thứ về một phân tử. Chúng chỉ cho ra một cấu trúc tĩnh đơn cho một protein, và không ghi lại được sự uốn cong và rung động diễn ra khi nó tương tác với các phân tử khác. Các thuật toán được huấn luyện trên cơ sở dữ liệu các cấu trúc đã biết, thể hiện nhiều nhất các cấu trúc dễ ánh xạ thực nghiệm thay vì sự đa dạng đầy đủ của tự nhiên. Kresten Lindorff-Larsen, một giáo sư tại Đại học Copenhagen, dự đoán rằng các thuật toán sẽ được sử dụng thường xuyên hơn và sẽ hữu ích, nhưng ông nói: “Chúng ta cũng cần học tốt hơn khi các phương pháp này thất bại.”
Ngoài cấu trúc protein gai, bài báo về Omicron của Subramaniam cũng bao gồm kết quả của một loại cấu trúc mà trí tuệ nhân tạo chưa thể chinh phục - một cấu trúc kết hợp giữa gai kết hợp với protein của người mà nó nhắm đến. Kết quả gợi ý rằng các biến đổi cấu trúc của biến thể cho phép nó kết hợp với tế bào chủ mạnh hơn đồng thời ít dễ bị kháng thể từ các biến thể trước đó, một sự kết hợp có vẻ giải thích tại sao Omicron có thể lây lan mạnh mẽ ngay cả trong cộng đồng đã tiêm vắc xin cao.
“Tiêu chuẩn vàng luôn là đo lường trực tiếp,” Subramaniam nói. “Nếu bạn đang xây dựng một chương trình dược phẩm tỷ đô, mọi người muốn biết điều gì là thực sự.” Đồng thời, ông nói công việc thực nghiệm của mình hiện nay thường được thông tin từ dự đoán của trí tuệ nhân tạo. “Nó đã thay đổi cách chúng tôi suy nghĩ,” Subramaniam nói.
Cập nhật, 13-1-2021, 14:15 ET: Phiên bản trước của bài viết này đã sai khi đề cập đến các mẫu ADN của Omicron.
Các thông tin tuyệt vời khác từ Mytour
- 📩 Tin tức mới nhất về công nghệ, khoa học và nhiều hơn nữa: Nhận tin tức của chúng tôi!
- Liệu một thế giới số có thể kết nối trực tiếp vào não bạn?
- Cơn bão trong tương lai có thể đến sớm hơn và kéo dài lâu hơn
- Metauniverse, cái gì chính xác là nó?
- Ban nhạc nhạc Marvel này có một câu chuyện nguồn gốc huyền thoại
- Cẩn thận với “công việc linh hoạt” và ngày làm việc không bao giờ kết thúc
- 👁️ Khám phá trí tuệ nhân tạo như chưa bao giờ có với cơ sở dữ liệu mới của chúng tôi
- 🎧 Âm thanh không ổn định? Hãy xem tai nghe không dây, loa thanh và loa Bluetooth yêu thích của chúng tôi
