
| Lưu huỳnh phân tử | |||
|---|---|---|---|
|
| |||
| Tên hệ thống | Lưu huỳnh Octatiocan | ||
| Nhận dạng | |||
| Số CAS | 10544-50-0 | ||
| PubChem | 66348 | ||
| MeSH | Cyclooctasulfur | ||
| ChEBI | 29385 | ||
| ChEMBL | 1235452 | ||
| Ảnh Jmol-3D | ảnh | ||
| SMILES | đầy đủ | ||
| Tham chiếu Gmelin | 2973 | ||
| UNII | 70FD1KFU70 | ||
| Thuộc tính | |||
| Bề ngoài | Tinh thể màu vàng. | ||
| Khối lượng riêng | 2.07 g cm | ||
| Điểm nóng chảy | 119 °C; 392 K; 246 °F | ||
| Điểm sôi | 444,6 °C; 717,8 K; 832,4 °F | ||
| log P | 6.117 | ||
| Nhiệt hóa học | |||
| Enthalpy hình thành ΔfH298 | 0 kJ·mol | ||
| Entropy mol tiêu chuẩn S298 | 32 J·mol·K | ||
| Các hợp chất liên quan | |||
| Hợp chất liên quan | Hexatian | ||
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). Tham khảo hộp thông tin | |||
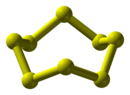
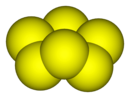
Lưu huỳnh là một chất vô cơ có công thức hóa học là S
8. Đây là một chất rắn màu vàng và là dạng phổ biến nhất của nguyên tố lưu huỳnh. Được sử dụng rộng rãi trong công nghiệp và tự nhiên.
Lưu huỳnh là nguyên tố phong phú thứ 10 về khối lượng trong vũ trụ và thứ 5 trên Trái Đất. Mặc dù thường được tìm thấy dưới dạng khoáng chất, lưu huỳnh tự nhiên trên Trái Đất đã được biết đến từ thời cổ đại và có nhiều ứng dụng lịch sử và văn hóa.
Cấu trúc phân tử
Lưu huỳnh có cấu trúc hình vương miện với nhóm đối xứng D4d. Độ dài liên kết S-S bằng nhau, khoảng 2,05 Å. Lưu huỳnh kết tinh thành ba dạng đa hình riêng biệt: trực thoi và hai dạng đơn tà, trong đó chỉ có hai dạng bền ở điều kiện tiêu chuẩn. Các dạng đa hình khác chỉ ổn định ở nhiệt độ từ 96 đến 115 °C ở áp suất 100 kPa. Lưu huỳnh cũng tạo ra các hợp chất có màu vàng và có nhiều ứng dụng khác nhau.
Phản ứng hóa học
Lưu huỳnh phản ứng với nhiều chất như Al, Fe, Cu, O2, Hg, C, Si,... tạo thành các muối sulfide tương ứng. Ví dụ như:
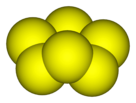

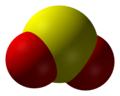
| + 8 8 |
|---|
Tuy nhiên, để đơn giản hóa, người ta thường sử dụng công thức S để biểu diễn lưu huỳnh, thay vì S8.
