1. Phương trình phản ứng hóa học:
Mg + Cl2 → MgCl2
Trong phản ứng này, magie (Mg) kết hợp với khí clo (Cl2) để tạo ra muối magie clo (MgCl2).
2. Dấu hiệu nhận diện phản ứng
Khi magie tiếp xúc với khí clo, một phản ứng hóa học xảy ra, trong đó magie bị oxi hóa và clo bị khử, tạo ra muối magie clo màu trắng.
Trước phản ứng, magie xuất hiện dưới dạng nguyên tử (Mg) và clo dưới dạng phân tử (Cl₂). Khi hai chất này phản ứng, magie bị oxi hóa thành ion magie dương (Mg²⁺) và clo bị khử thành ion clo âm (Cl⁻). Magie mất hai electron để tạo thành ion dương, còn clo nhận thêm một electron và trở thành ion âm. Các ion này kết hợp để hình thành muối magie clo, có công thức hóa học là MgCl₂, và thường xuất hiện dưới dạng bột hoặc tinh thể màu trắng.
Tóm lại, khi magie phản ứng với khí clo, magie bị oxi hóa thành ion magie dương (Mg²⁺) và clo bị khử thành ion clo âm (Cl⁻). Các ion này kết hợp để tạo ra muối magie clo (MgCl₂) màu trắng.
3. Điều kiện để phản ứng xảy ra
Để phản ứng giữa magie và clo diễn ra, cần phải đáp ứng một số điều kiện cần thiết, bao gồm cả yếu tố nhiệt độ và sự hiện diện của các chất phản ứng.
Trước hết, điều kiện nhiệt độ đóng vai trò quan trọng để đảm bảo phản ứng xảy ra nhanh và hiệu quả. Thông thường, nhiệt độ được duy trì ở mức phòng, khoảng 25 độ Celsius. Nhiệt độ này giúp phản ứng diễn ra ở tốc độ hợp lý và đảm bảo an toàn.
Tiếp theo, phản ứng yêu cầu sự có mặt của khí clo (Cl₂) và magie (Mg). Khí clo là chất oxi hóa trong phản ứng, trong khi magie là chất bị oxi hóa. Khi hai chất này tương tác, magie sẽ chuyển thành ion magie dương (Mg²⁺) và clo sẽ chuyển thành ion clo âm (Cl⁻). Sự kết hợp của ion magie dương và ion clo âm tạo ra muối magie clo (MgCl₂) có màu trắng.
Tóm lại, để phản ứng giữa magie và clo xảy ra, cần duy trì điều kiện nhiệt độ ở mức phòng, khoảng 25 độ Celsius. Thêm vào đó, sự hiện diện của khí clo (Cl₂) và magie (Mg) là yếu tố cần thiết để tạo ra muối magie clo (MgCl₂).
4. Tính chất hóa học
Magie (Mg) là một chất khử mạnh mẽ, có khả năng mất electron để chuyển thành ion magie dương (Mg²⁺). Dưới đây là công thức hóa học mô tả quá trình khử của magie:
Mg → Mg²⁺ + 2e⁻
a. Tác dụng với phi kim:
Magie có khả năng phản ứng với nhiều loại phi kim khác nhau. Ví dụ, khi magie phản ứng với khí cacbon dioxide (CO₂), nó khử CO₂ thành oxit magie (MgO) bằng cách mất electron:
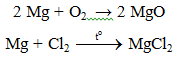
Điều này chứng tỏ khả năng khử mạnh mẽ của magie khi phản ứng với các phi kim khác.
Lưu ý:
- Vì Mg có độ ái lực cao với oxy: 2Mg + CO2 → MgO, nên không nên sử dụng tuyết cacbonic để dập tắt lửa magie.
b. Phản ứng với axit
Magie (Mg) phản ứng với các dung dịch axit như HCl, H2SO4 và HNO3 theo những phương trình sau:
Khi phản ứng với dung dịch HCl (axit clohidric) loãng:
Mg + 2HCl → MgCl2 + H2
Trong phản ứng này, magie kết hợp với axit clohidric để tạo ra muối magie clorua (MgCl2) và khí hidro (H2).
Khi phản ứng với dung dịch H2SO4 (axit sunfuric) loãng:
Mg + H2SO4 → MgSO4 + H2
Trong trường hợp này, magie phản ứng với axit sunfuric để tạo ra muối magie sunfat (MgSO4) và khí hidro (H2).
Khi sử dụng dung dịch HNO3 (axit nitric):
4Mg + 10HNO3 → 4Mg(NO3)2 + NH4NO3 + 3H2O
Phản ứng này là một phản ứng oxi hóa-khử phức tạp. Magie kết hợp với axit nitric tạo thành muối magie nitrat (Mg(NO3)2), muối amoni nitrat (NH4NO3) và nước.
Lưu ý rằng phản ứng với axit nitric sinh ra một số sản phẩm phức tạp bổ sung như muối amoni nitrat và nước.
Tóm lại, magie có khả năng phản ứng với các dung dịch axit như HCl, H2SO4 và HNO3 để tạo ra muối magie clorua, magie sunfat và magie nitrat, kèm theo khí hidro và các sản phẩm phụ phức tạp khác tùy thuộc vào loại axit và điều kiện phản ứng.
5. Thực hiện phản ứng
Để tiến hành phản ứng giữa magie và khí clo, bạn có thể thực hiện các bước sau:
- Chuẩn bị các vật liệu và thiết bị cần thiết: Magie (Mg) và khí clo (Cl₂). Đảm bảo làm việc trong môi trường an toàn, có thông gió đầy đủ và kiểm soát chặt chẽ các chất nguy hiểm.
- Chuẩn bị một hệ thống để nung nóng khí clo: Sử dụng một bình chứa hoặc ống nghiệm kín để đựng khí clo. Áp dụng nhiệt để nung nóng khí clo trong bình hoặc ống nghiệm. Đảm bảo an toàn khi làm việc với khí clo do tính chất độc hại và kích thích mạnh của nó.
- Đưa magie vào bình chứa hoặc ống nghiệm có khí clo: Đảm bảo rằng bình hoặc ống nghiệm đã được nung nóng và đang chứa khí clo trước khi thêm magie. Khi magie tiếp xúc với khí clo, sẽ xảy ra phản ứng ngay lập tức.
- Quan sát sự phản ứng: Ngay khi magie tiếp xúc với khí clo, phản ứng sẽ xảy ra ngay lập tức. Theo dõi sự thay đổi màu sắc, nhiệt độ hoặc các hiện tượng khác để nhận biết phản ứng đã diễn ra.
- Thu được muối: Phản ứng sẽ tạo ra muối magie clo (MgCl2), có thể tồn tại dưới dạng rắn hoặc tan trong dung môi phù hợp để tạo thành dung dịch muối.
Lưu ý rằng làm việc với khí clo và magie cần phải cực kỳ cẩn thận và tuân thủ các quy định an toàn. Hãy làm việc trong khu vực thông gió tốt và sử dụng thiết bị bảo hộ cá nhân như găng tay, kính bảo hộ và áo bảo hộ để đảm bảo an toàn.
6. Những thông tin bạn có thể tham khảo
Magie (Mg) là một kim loại với tính khử mạnh mẽ, vì vậy nó dễ dàng phản ứng với các chất có tính oxi hóa cao như oxi (O₂) và clo (Cl₂). Dưới đây là một số phản ứng quan trọng mà magie tham gia:
Phản ứng với oxi (O₂):
2Mg + O₂ → 2MgO
Khi magie phản ứng với oxi, nó tạo ra oxit magie (MgO). Magie mất electron cho oxi, trong khi oxi nhận electron và trở thành ion oxit (O²⁻). Đây là một phản ứng oxi hóa-khử, trong đó magie là chất khử và oxi là chất oxi hóa.
Phản ứng với clo (Cl₂):
Mg + Cl₂ → MgCl₂
Khi magie phản ứng với khí clo, tạo ra muối magie clo (MgCl₂). Magie sẽ mất electron và hình thành ion magie (Mg²⁺), trong khi clo nhận electron để trở thành ion clo (Cl⁻). Magie đóng vai trò chất khử, còn clo là chất oxi hóa.
Hai phản ứng này chứng minh sức mạnh khử của magie, khi nó dễ dàng chuyển đổi thành ion dương và phản ứng với các chất oxi hóa mạnh như oxi và clo.
Khi làm việc với magie và các chất oxi hóa mạnh như oxi và clo, cần tuân thủ các biện pháp an toàn và làm việc trong khu vực thông gió tốt.
7. Bài tập thực hành
Ví dụ 1: Khi magie phản ứng với clorua, sản phẩm thu được sẽ có màu gì?
A. Màu xanh lục.
B. Màu trắng.
C. Màu đen.
D. Màu nâu đen.
Hướng dẫn giải:
Khi magie (Mg) phản ứng với clorua (Cl⁻), sản phẩm tạo ra là muối magie clorua (MgCl₂) và không có sự thay đổi màu sắc rõ rệt. Do đó, đáp án đúng là B - màu trắng.
Ví dụ 2: Thực hiện các thí nghiệm sau đây:
(1) Đưa lá hợp kim Zn - Cu vào dung dịch H2SO4 loãng.
(2) Đưa lá Pb vào dung dịch AgNO3.
(3) Đưa lá Zn vào dung dịch HNO3 loãng.
(4) Đốt dây Mg trong khí Cl2.
Số thí nghiệm xảy ra ăn mòn hóa học là
A. 1
B. 2
Câu 3
Đáp án là 4
Hướng dẫn giải chi tiết:
Đáp án chính là D
Ví dụ 3: Khi cho Mg phản ứng với khí clo dư, ta thu được muối X. Hòa tan muối X trong nước để được dung dịch Y. Nếu cho AgNO3 dư vào dung dịch Y, ta sẽ thu được kết tủa Z. Kết tủa Z là gì?
A. Mg
B. MgCl2
C. AgCl
D. Ag2O
Hướng dẫn chi tiết:
Đáp án đúng là C. Kết tủa Z chính là AgCl.
Khi magiê (Mg) phản ứng với khí clo (Cl2), tạo thành muối magiê clorua (MgCl2) theo phương trình: Mg + Cl2 → MgCl2.
Muối MgCl2 được hòa tan vào nước, tạo ra dung dịch Y.
Khi dung dịch Y chứa MgCl2 được phản ứng với AgNO3 dư, sẽ tạo kết tủa AgCl và muối Mg(NO3)2 theo phương trình: MgCl2 + 2AgNO3 → 2AgCl + Mg(NO3)2.
Do đó, kết tủa Z chính là AgCl.
