1. Phương trình phản ứng hóa học
Ca(HCO3)2 + NaOH → CaCO3 kết tủa + H2O + NaHCO3
2. Hiện tượng của phản ứng
- Phản ứng tạo ra kết tủa trắng
3. Cách thực hiện phản ứng
Cho Ca(HCO3)2 phản ứng với NaOH.
4. Điều kiện để phản ứng xảy ra
Phản ứng diễn ra ở điều kiện bình thường
5. Đặc điểm của các chất tham gia phản ứng
5.1. NaOH
* Tính chất vật lý: NaOH là một chất rắn, không màu, dễ tan chảy và có khả năng hút ẩm mạnh, dẫn đến tính chất ăn mòn. NaOH hòa tan tốt trong nước và giải phóng một lượng nhiệt lớn, vì vậy cần thận trọng khi hòa tan trong nước.
* Tính chất hóa học:
- Phân li hoàn toàn thành ion khi hòa tan trong nước
- Dung dịch NaOH làm quỳ tím chuyển sang màu xanh
- Dung dịch NaOH phản ứng với axit và oxit axit để tạo thành muối và nước
- Dung dịch NaOH khi tác dụng với dung dịch muối sẽ tạo ra muối mới và bazơ mới
* Ứng dụng: NaOH được sử dụng trong sản xuất xà phòng, chế biến phẩm nhuộm, sợi tổng hợp, và nhiều ứng dụng khác
5.2. Ca(HCO3)2
* Tính chất hóa học:
- Phản ứng với axit mạnh
- Phản ứng với dung dịch bazơ
- Bị phân hủy khi chịu nhiệt
6. Bài tập ứng dụng liên quan
Bài 1: Đặt một miếng natri nhỏ lên một tờ giấy thấm, gấp lại thành hình chiếc thuyền. Đặt chiếc thuyền giấy này vào một chậu nước có vài giọt phenolphtalein.
Dự đoán hiện tượng có thể quan sát được trong thí nghiệm sau đây:
1. Chiếc thuyền di chuyển xung quanh trên mặt nước
2. Chiếc thuyền bị cháy
3. Nước chuyển sang màu hồng
4. Miếng natri nóng chảy
Trong các dự đoán nêu trên, có bao nhiêu dự đoán chính xác?
A. 1 dự đoán chính xác
B. 2 dự đoán chính xác
C. 3 dự đoán chính xác
D. 4 dự đoán chính xác
Hướng dẫn giải chi tiết: Chọn D. Có 4 dự đoán đúng. Giải thích:
- Chiếc thuyền làm bằng giấy thấm nước khiến mẫu natri phản ứng với nước. Phương trình phản ứng: 2Na + 2H2O → 2NaOH + H2
- Khí H2 sinh ra làm đẩy mẫu natri và khiến chiếc thuyền di chuyển vòng quanh chậu nước
- Phản ứng tỏa nhiệt nhiều, làm chiếc thuyền cháy, mẫu natri nóng chảy và cuộn lại (do sức căng bề mặt)
- Vì NaOH là dung dịch bazơ nên khi thêm phenolphtalein vào, dung dịch sẽ chuyển sang màu hồng.
Câu 2: Khi cho dung dịch NaOH dư vào cốc chứa dung dịch Ca(HCO3)2 trong suốt, hiện tượng gì sẽ xảy ra trong cốc?
A. Xuất hiện hiện tượng sủi bọt khí
B. Xuất hiện hiện tượng kết tủa trắng
C. Không có hiện tượng gì xảy ra
D. Xuất hiện hiện tượng kết tủa trắng và bọt khí.
Hướng dẫn giải chi tiết: Chọn B. Khi cho dung dịch NaOH dư vào cốc chứa dung dịch Ca(HCO3)2 trong suốt, hiện tượng kết tủa trắng CaCO3 sẽ xảy ra trong cốc.
Ca(HCO3)2 + 2NaOH → CaCO3 kết tủa + 2H2O + Na2CO3
Câu 3: Các hang động với những nhũ đá tuyệt đẹp hình thành nhờ hai quá trình chính:
- Quá trình (1): Phá vỡ đá vôi do tác động của nước mưa chứa khí cacbonic, dẫn đến sự hòa tan và tạo ra muối canxi hidrocacbonat Ca(HCO3)2.
- Quá trình (2): Canxi hidrocacbonat bị phân hủy khi chảy qua các khe nứt trong hang động, tạo thành canxi cacbonat, khí cacbonic CO2 và nước, từ đó hình thành các nhũ đá.
a, Viết công thức hóa học của canxi hidrocacbonat được cấu tạo từ canxi và nhóm CO3 (II).
b, Viết phương trình hóa học cho phản ứng phân hủy canxi hidrocacbonat.
c, Xác định phần trăm khối lượng của các nguyên tố trong Ca(HCO3)2.
d, Tính khối lượng và thể tích khí cacbonic sinh ra khi phân hủy 81 gam Ca(HCO3)2. Biết khối lượng canxi cacbonat và nước lần lượt là 50 gam và 9 gam.
e, Nếu phân hủy 121,5 gam Ca(HCO3)2 thì thu được bao nhiêu gam khí cacbonic?
Dữ liệu: H = 1; C = 12; N = 14; O = 16; K = 39; Ca = 40.
Hướng dẫn giải chi tiết:
a, Công thức hóa học của canxi cacbonat là CaCO3.
d, Phương trình phản ứng phân hủy: Ca(HCO3)2 → CaO + H2O + 2CO2. Áp dụng định luật bảo toàn khối lượng:
=> mCO2 = 81 - (50 + 9) = 22 gam
nCO2 = 22/44 = 0,5 mol => VCO2 = 0,5 * 22,4 = 11,2 lít
e, Phản ứng phân hủy: Ca(HCO3)2 → CaO + H2O + 2CO2
nCa(HCO3)2 = 121,5 : 162 = 0,75 mol => mCO2 = 44 * 1,5 = 66 gam.
Câu 4: Công dụng nào dưới đây không phải của CaCO3:
A. Sử dụng CaCO3 để làm vôi quét tường
B. Sử dụng CaCO3 làm vật liệu xây dựng
C. Sử dụng CaCO3 để sản xuất xi măng
D. Sử dụng CaCO3 để tạo bột nhẹ pha sơn
Đáp án: Chọn D. Việc làm vôi quét tường không phải là công dụng của CaCO3. Việc quét tường thực chất dùng vôi tôi Ca(OH)2, được tạo ra khi CaO phản ứng với nước.
Câu 5: Có ba lọ không nhãn, mỗi lọ chứa một trong ba chất rắn màu trắng: CaCO3, Ca(OH)2, hoặc CaO. Hãy xác định chất trong mỗi lọ bằng phương pháp hóa học. Viết phương trình hóa học tương ứng.
Lời giải:
Lấy một ít của mỗi chất rắn làm mẫu thử, đánh số thứ tự từng mẫu, sau đó cho chúng vào nước.
- Chất nào không tan trong nước chính là CaCO3.
- Chất nào phản ứng với nước và làm ống nghiệm nóng lên là CaO.
Phương trình hóa học: CaO + H2O → Ca(OH)2
- Chất nào chỉ hòa tan một phần trong dung dịch màu trắng và tạo một phần kết tủa lắng xuống đáy là Ca(OH)2.
Câu 6: Khi hòa tan hoàn toàn 19,2 gam hỗn hợp chứa CaCO3 và MgCO3 trong dung dịch HCl dư, thấy khí CO2 thoát ra có thể tích V (lít) ở điều kiện tiêu chuẩn và dung dịch sau phản ứng còn lại 21,4 gam hỗn hợp muối. Xác định thể tích V.
A. V = 3,29 lít
B. V = 3,63 lít
C. V = 4,48 lít
D. V = 5,06 lít
Câu 7: Cho 10 gam CaCO3 phản ứng với axit HCl dư, sau đó dẫn khí sinh ra qua 60 gam dung dịch NaOH 10% để xảy ra phản ứng hoàn toàn, thu được dung dịch B. Khối lượng muối trong dung dịch B là:
A. Khối lượng muối trong dung dịch B là 5,5 gam
B. Khối lượng muối trong dung dịch B là 15,5 gam
C. Khối lượng muối trong dung dịch B là 9,5 gam
D. Khối lượng muối trong dung dịch B là 5,9 gam
Hướng dẫn giải: Chọn C. Khối lượng muối trong dung dịch B là 15,5 gam
Khi CaCO3 phản ứng với HCl dư: nCO2 = nCaCO3 = 10/100 = 0,1 mol
Hấp thụ 0,1 mol CO2 vào 0,15 mol NaOH:
Ta có 1 < nOH-/nCO2 = 0,15/0,1 = 1,5 < 2 => Tạo Na2CO3 và NaHCO3.
=> m muối = 0,05 × 106 + 0,05 × 84 = 9,5 gam
Câu 8: Khi cho 20 gam CaCO3 phản ứng với axit HCl dư, rồi dẫn khí sinh ra qua 120 gam dung dịch NaOH 10% để xảy ra phản ứng hoàn toàn, thu được dung dịch B. Khối lượng muối trong dung dịch B là:
A. Khối lượng muối là 19 gam
B. Khối lượng muối là 20 gam
C. Khối lượng muối là 21 gam
D. Khối lượng muối là 22 gam
Đáp án: Chọn A. Khối lượng muối trong dung dịch B là 19 gam
Câu 9: Canxi cacbonat (CaCO3) là thành phần chính của đá vôi. Khi nung đá vôi, xảy ra phản ứng hóa học sau đây:
Canxi cacbonat → Canxi oxit + Cacbon đioxit
Biết rằng khi nung 280 kg đá vôi tạo ra 140 kg canxi oxit CaO (vôi sống) và 110 kg khí cacbon dioxit CO2
a. Viết công thức liên quan đến khối lượng các chất trong phản ứng
b. Tính tỷ lệ phần trăm khối lượng canxi cacbonat có trong đá vôi
Giải chi tiết:
a. Phương trình hóa học:
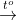
Dựa theo định luật bảo toàn khối lượng, ta có:
mCaCO3 = mCaO + mCO2
b. mCaCO3 = 140 + 110 = 250 (kg)
Tỷ lệ phần trăm khối lượng canxi cacbonat có trong đá vôi là:
%mCaCO3 = (250 / 280) × 100% = 89,3%
Câu 10: Để sản xuất vôi sống CaO, ta nung đá vôi, mà thành phần chính là canxi cacbonat CaCO3.
a. Viết phương trình hóa học của phản ứng xảy ra
b. Từ 1 tấn đá vôi chứa 80% canxi cacbonat, có thể sản xuất được bao nhiêu tấn vôi sống.
Giải chi tiết:
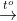
b. Một tấn vôi sống chứa 0,8 tấn CaCO3. Do đó, từ 1 tấn vôi sống với 80% canxi cacbonat, có thể sản xuất được 0,448 tấn CaO.
Đây là bài viết của Mytour về phản ứng Ca(HCO3)2 + NaOH hay Ca(HCO3)3 ra CaCO3. Hy vọng bài viết này sẽ cung cấp thông tin hữu ích, giúp bạn nắm vững kiến thức về phản ứng và áp dụng vào các bài tập vận dụng, luyện tập. Xin chân thành cảm ơn!
