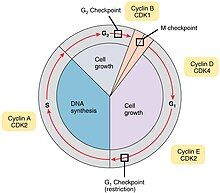
Quản lý chu kỳ tế bào là các cơ chế kiểm soát trong tế bào nhằm đảm bảo quá trình phân bào diễn ra chính xác. Các điểm kiểm soát này theo dõi sự tiến triển của chu kỳ tế bào và ngăn chặn tế bào tiếp tục nếu có sai sót. Ba điểm chính bao gồm: điểm kiểm soát G1, điểm kiểm soát G2/M và điểm kiểm soát thoi vô sắc. Các kinase phụ thuộc cyclin và cyclin điều hòa sự hoạt động của các điểm kiểm soát này, đảm bảo các sự kiện trong chu kỳ tế bào diễn ra đúng cách.
Chức năng
Tất cả sự sống đều bắt nguồn từ quá trình tăng trưởng và phân chia tế bào. Chu kỳ tế bào ở sinh vật nhân thực gồm bốn giai đoạn chính: G1, pha S, G2, và pha M (nguyên phân). Trong khi chu kỳ tế bào của sinh vật nhân sơ diễn ra đơn giản hơn, ở sinh vật nhân thực, quá trình này phức tạp hơn và được điều chỉnh bởi hệ thống kiểm soát chu kỳ tế bào. Hệ thống này như một chiếc đồng hồ, điều chỉnh thời gian cho từng pha và phản ứng với thông tin kiểm soát. Điểm kiểm soát nhận diện các lỗi trong tái bản DNA hoặc phân ly nhiễm sắc thể và sử dụng cơ chế tín hiệu để ngừng chu kỳ tế bào nếu cần thiết hoặc kích hoạt cơ chế tự hủy. Các điểm kiểm soát dùng cơ chế nhận diện-tín hiệu-phản ứng để duy trì sự ổn định của quá trình phân bào.
Trong đa số các tế bào nhân chuẩn, chu kỳ tế bào có ba điểm kiểm soát chính. Điểm kiểm soát đầu tiên nằm ở cuối pha G1, gọi là điểm giới hạn (restriction point hay restriction checkpoint - RP), nơi tế bào chuyển vào pha S và bắt đầu tự nhân đôi DNA. Điểm kiểm soát thứ hai là điểm kiểm soát G2/M, nơi các cơ chế kiểm soát kích hoạt quá trình nguyên phân và sắp xếp nhiễm sắc thể trên thoi vô sắc. Điểm kiểm soát thứ ba là điểm chuyển tiếp kỳ giữa-kỳ sau, nơi hệ thống kiểm soát kích hoạt sự phân chia các nhiễm sắc tử chị em trong nhiễm sắc thể kép. Các điểm kiểm soát này hoạt động bằng cách điều hòa các protein kinase gọi là cyclin-dependent kinase (CDKs) thông qua sự kết hợp với các cyclin để tạo thành phức hợp cyclin-CDK, từ đó kích hoạt các pha khác nhau của chu kỳ tế bào.
Điểm giới hạn
Điểm kiểm soát đầu tiên trong chu kỳ tế bào nằm ở cuối pha G1 và trước pha S. Điểm này quyết định liệu tế bào có tiếp tục phân chia hay không. Nhiều tế bào không vượt qua điểm giới hạn và vào trạng thái 'nghỉ' ở pha G0. Ví dụ, tế bào gan chỉ phân chia một hay hai lần trong năm. Điểm giới hạn đóng vai trò quan trọng trong việc ngăn chặn chu kỳ tế bào nếu điều kiện môi trường không phù hợp hoặc tế bào cần thêm thời gian ở pha G0. Trong động vật, điểm này gọi là 'điểm giới hạn', trong khi ở nấm men, nó được gọi là 'điểm bắt đầu'. Điểm giới hạn chủ yếu được điều khiển bởi chất ức chế CDK p16 (CKI- p16 - CDK inhibitor p16), ngăn cản CDK4/6 tương tác với cyclin D1 và tiếp tục chu kỳ tế bào. Khi biểu hiện của cyclin D tăng cao, điểm kiểm soát này bị vượt qua do cyclin D tương tác với CDK4/6, dẫn đến hình thành phức hợp CDK4/6-CYCLIN D, phosphat hóa các chất ức chế khối u (Rb) và loại bỏ sự ức chế của các nhân tố phiên mã E2F. E2F sau đó kích hoạt sự biểu hiện của cyclin E, tương tác với CDK2 để thúc đẩy sự chuyển tiếp giữa pha G1 và pha S.
Tóm lại, chất ức chế CDK p16 ngăn cản các CDK khác kết hợp với cyclin D. Tuy nhiên, khi tế bào kích thích tăng trưởng, cyclin D tăng mạnh, áp đảo các p16 và cho phép CDK kết hợp với cyclin D để hình thành phức hợp. Phức hợp này phosphat hóa các chất ức chế khối u (Rb), làm mất hoạt tính của chúng đối với nhân tố phiên mã E2F. E2F sau đó thúc đẩy sự chuyển tiếp từ pha G1 sang pha S.
Điểm kiểm soát G2/M
Điểm kiểm soát thứ hai trong chu kỳ tế bào nằm ở cuối pha G2 và có nhiệm vụ điều khiển sự khởi đầu của pha nguyên phân hay pha M. Để vượt qua điểm kiểm soát này, tế bào cần kiểm tra một số yếu tố để đảm bảo sẵn sàng cho nguyên phân. Khi điểm kiểm soát này được vượt qua, tế bào khởi động nhiều quá trình phân tử để kích hoạt pha nguyên phân. Các CDK liên quan đến điểm kiểm soát này được kích hoạt nhờ sự phosphat hóa bởi 'Nhân tố xúc tiến trưởng thành' (Maturation Promoting Factor - MPF) hay 'Nhân tố xúc tiến nguyên phân' (Mitosis Promoting Factor - MPF).
Điểm kiểm soát này liên quan đến việc kích hoạt enzyme phosphatase gọi là Cdc25, enzyme này loại bỏ các phosphate ức chế trong phức hợp MPF khi điều kiện cho phép. Tuy nhiên, DNA thường xuyên bị tổn thương và hư hỏng trước khi nguyên phân bắt đầu, vì vậy chu kỳ tế bào sẽ bị ngăn chặn nếu có sự hư hỏng để tránh truyền lỗi sang các tế bào con. Điều này xảy ra qua việc hoạt hóa Cdc25 phosphatase (nhờ phosphat hóa từ các enzyme kinase khác).
Điểm chuyển tiếp kỳ giữa-kỳ sau
Điểm kiểm soát thoi vô sắc xuất hiện trong kỳ giữa của nguyên phân khi tất cả các nhiễm sắc thể kép đã được hoặc sẽ được sắp xếp sao cho tâm động thẳng hàng trên mặt phẳng xích đạo và chịu sức căng từ hai cực của tế bào qua các sợi thoi vô sắc gắn vào tâm động. Sức căng này được cơ chế kiểm soát nhận diện và kích hoạt kỳ sau của nguyên phân, bắt đầu bằng việc APC/C xúc tiến sự tách rời các nhiễm sắc tử chị em trong mỗi nhiễm sắc thể kép.
Cơ chế nhận diện hiện vẫn chưa được hiểu rõ; tuy nhiên, một số protein như Mad2 được tâm động của nhiễm sắc thể kép triệu tập vào thời điểm này. Mad2 là một protein có chức năng ngăn chặn APC/C phân giải cohesin, và chỉ khi tâm động được gắn kết hoàn toàn với sợi thoi, Mad2 mới bị bất hoạt. Điều này có nghĩa là APC/C chỉ hoạt động khi tất cả các tâm động đã gắn kết với sợi thoi, từ đó quá trình phân giải cohesin diễn ra và sau 20 phút, kỳ sau của nguyên phân bắt đầu.
Cơ chế nhận diện này cho phép cyclin B bị phân giải nhờ vào chuỗi amino acid gọi là 'hộp phá hủy' (destruction box hay D-box), và hộp này được đánh dấu bởi phức hợp xúc tiến kỳ sau (APC/C) để tiêu thể nhận diện và phân giải. Khi cyclin B bị phân giải, nó không còn ức chế được APC/C, giúp các phức hợp này tự do kích hoạt quá trình phân giải securin. Securin là một protein ức chế separase, một phức hợp protein có chức năng tách các nhiễm sắc tử chị em khỏi nhiễm sắc thể kép. Khi securin bị phân giải bởi tiêu thể nhờ ubiquitin hóa, separase sẽ được kích hoạt để thực hiện việc tách rời các nhiễm sắc tử.
- Điểm kiểm soát sau sao chép DNA
- Vị trí kích hoạt hóa sinh trong chu kỳ tế bào
- Phương pháp phân tích chu kỳ tế bào
- Điểm kiểm soát G2-M liên quan đến hỏng DNA
- Bruce Alberts (2008). “17”. Molecular Biology of the Cell. Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, Peter Walter. Garland Science, Taylor & Francis Group. ISBN 978-0-8153-4106-2.
- Harvey Lodish (2003). “22”. Molecular Cell Biology. Arnold Berk, Paul Matsudaira, Chris A. Kaiser, Monty Krieger, Matthew P. Scott, Lawrence Zipursky, James Darnell. ISBN 0716743663.
Chú thích
Cước chú
Nguồn tài liệu
Mẫu:Chu kỳ tế bào
