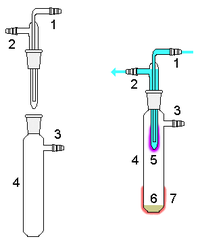
Thăng hoa là quá trình chuyển đổi vật chất từ thể rắn trực tiếp thành thể khí mà không qua trạng thái lỏng. Đây là một quá trình hấp thụ nhiệt diễn ra dưới nhiệt độ và áp suất thấp hơn điểm ba của chất, tức là áp suất thấp nhất mà chất có thể tồn tại dưới dạng lỏng. Quá trình ngược lại với thăng hoa là ngưng kết, khi chất chuyển từ khí thành rắn. Thăng hoa cũng được dùng để chỉ sự chuyển đổi từ rắn sang khí (thăng hoa), sau đó là từ khí trở lại rắn (ngưng kết). Khi chất lỏng bay hơi dưới điểm sôi, nó xảy ra trên bề mặt; nếu ở điểm sôi, sẽ có sự sôi và hình thành bọt khí trong chất lỏng. Trong khi đó, chuyển từ rắn sang khí luôn xảy ra dưới dạng thăng hoa trên bề mặt chất rắn.
Ở áp suất bình thường, hầu hết các hợp chất hóa học và nguyên tố tồn tại ở ba trạng thái khác nhau tại các nhiệt độ khác nhau. Trong các trường hợp này, sự chuyển từ rắn sang khí thường phải qua trạng thái lỏng trung gian. Tuy nhiên, áp suất ở đây là áp suất riêng phần của chất, không phải áp suất tổng thể như áp suất khí quyển. Vì vậy, các chất rắn có áp suất hơi có thể đo được ở một nhiệt độ nhất định thường có khả năng thăng hoa trong không khí (như băng nước dưới 0 °C). Đối với một số chất như cacbon và arsenic, thăng hoa có thể xảy ra dễ dàng hơn sự bay hơi của chất lỏng vì áp suất điểm ba của chúng rất cao, làm cho việc chuyển chúng thành dạng lỏng rất khó khăn.
Thuật ngữ thăng hoa chỉ quá trình chuyển đổi trạng thái vật lý của một chất từ rắn sang khí mà không qua thể lỏng, không phải là sự phản ứng hóa học. Ví dụ, khi đun nóng nhôm chloride để tạo ra hydro chloride và amoniac, đó là phản ứng hóa học chứ không phải thăng hoa. Tương tự, khi sáp parafin của nến cháy, nó biến thành carbon dioxide và hơi nước qua phản ứng với oxy, cũng không phải là thăng hoa.
Thăng hoa xảy ra khi chất hấp thụ nhiệt, cung cấp đủ năng lượng để các phân tử vượt qua lực hút của các phân tử lân cận và chuyển thành pha khí. Vì quá trình này yêu cầu thêm năng lượng, nên nó là một quá trình thu nhiệt. Entanpi thăng hoa, hay nhiệt thăng hoa, có thể được tính bằng tổng của entanpi nóng chảy và entanpi hóa hơi.
Các chất thường gặp liên quan đến hiện tượng thăng hoa bao gồm: băng phiến (naftalin chống mọt), băng khô, xăng khô, băng, tuyết, iod,...
Ví dụ minh họa
Cacbon dioxit

Cacbon dioxit (băng khô) chuyển thẳng từ rắn sang khí ở mọi điều kiện dưới điểm ba, tức là ở nhiệt độ −78,5 °C (194,65 K, −109,30 °F) tại áp suất khí quyển. Tuy nhiên, ở nhiệt độ và áp suất cao hơn điểm ba (5,1 atm, −56,6 °C), cacbon dioxit có thể nóng chảy thành CO2 lỏng.
Nước
Băng và tuyết cũng có thể thăng hoa, mặc dù chậm hơn, ở nhiệt độ dưới điểm đông đặc/nóng chảy, theo đường đẳng nhiệt 0 °C cho các áp suất riêng phần thấp hơn áp suất điểm ba 612 Pa (0,00604 atm). Trong quá trình sấy đông khô, vật liệu cần loại nước được đông lạnh và sau đó nước được thăng hoa dưới điều kiện áp suất giảm hoặc chân không.
Naphthalen



Băng phiến, một hợp chất hữu cơ thường thấy trong thuốc chống côn trùng, dễ thăng hoa vì cấu trúc phân tử không phân cực và chỉ có lực van der Waals giữ các phân tử lại với nhau. Băng phiến là chất rắn thăng hoa ở áp suất khí quyển tiêu chuẩn với nhiệt độ thăng hoa khoảng 80 °C (176 °F). Ở nhiệt độ thấp, áp suất hơi của nó, 1 mmHg tại 53 °C, đủ cao để chuyển từ rắn sang khí. Trên các bề mặt đủ lạnh, hơi băng phiến sẽ chuyển thành dạng rắn và hình thành các tinh thể dạng kim.
Các chất khác
Khi được đun nóng nhẹ, iod phát ra khói, mặc dù hiện tượng này xảy ra ở nhiệt độ trên điểm ba và không phải là thăng hoa thực sự. Iod lỏng có thể được thu được ở áp suất khí quyển bằng cách điều chỉnh nhiệt độ ngay trên điểm nóng chảy của nó. Trong khoa học pháp y, hơi iod có thể được sử dụng để hiện dấu vân tay ẩn trên giấy. Arsen cũng có thể thăng hoa ở nhiệt độ cao.
Cadmi và kẽm không thích hợp cho sử dụng trong chân không vì chúng thăng hoa dễ dàng hơn các vật liệu thông thường trong điều kiện này.
Ứng dụng

Trong kỹ thuật cắt laser thăng hoa, tia laser với công suất xung cao làm cho vật liệu chuyển từ trạng thái rắn trực tiếp thành khí mà không cần phải nóng chảy trước. Kết quả là những đường cắt rất sạch, không có xỉ và các cạnh sắc nét.
Các ứng dụng khác của thăng hoa bao gồm sấy đông khô thực phẩm, một phương pháp sấy không sử dụng nhiệt, giúp bảo vệ chất lượng thực phẩm tốt hơn so với các phương pháp khác. Công nghệ in thăng hoa là một kỹ thuật in số sử dụng màu sắc đầy đủ với nền polyester hoặc lớp phủ polymer. Trong máy in thăng hoa, sáp nhuộm màu thay thế mực, được làm nóng gần 200°C bởi các vi điện trở trên đầu in, chuyển từ rắn sang khí ngay lập tức, sau đó nguội và trở lại trạng thái rắn trên tấm in. Phương pháp này tận dụng tính chất trong suốt của sáp, cho phép in màu chính xác với ba lớp sáp (vàng, hồng cánh sen và xanh lơ) tạo ra tổng cộng 16,73 triệu màu.
Thăng hoa cũng được sử dụng như một phương pháp thay thế cho tái kết tinh trong việc tinh chế các sản phẩm hóa học. Một ví dụ về ứng dụng của thăng hoa trong ngành hóa phóng xạ là tinh chế một nuclide để xác định chu kỳ bán rã của đồng vị Se. Trong phòng thí nghiệm, thăng hoa thường được sử dụng để tinh chế các hợp chất như ferrocene, pyrogallol, naphthalen, phthalic anhydride, camphor, anthraquinone, acid salicylic, acid benzoic, urani hexafluoride và một số kim loại.
- Bay hơi
- Entanpi thăng hoa
- Ngưng kết, quá trình chuyển pha ngược với thăng hoa
Tư liệu liên quan đến Thăng hoa trên Wikimedia Commons
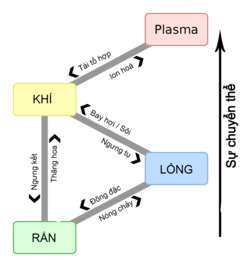
Trạng thái vật chất | ||
|---|---|---|
| Trạng thái |
| |
| Năng lượng thấp |
| |
| Năng lượng cao |
| |
| Các trạng thái khác |
| |
| Chuyển pha |
| |
| Đại lượng |
| |
| Khái niệm |
| |
| Danh sách |
| |
