1. Xác định hai chất X và Y trong sơ đồ chuyển hoá: Glucozơ → X → Y → CH3COOH.
X là etanol (C2H5OH), một hợp chất quan trọng trong nhiều quy trình hóa học và công nghiệp.
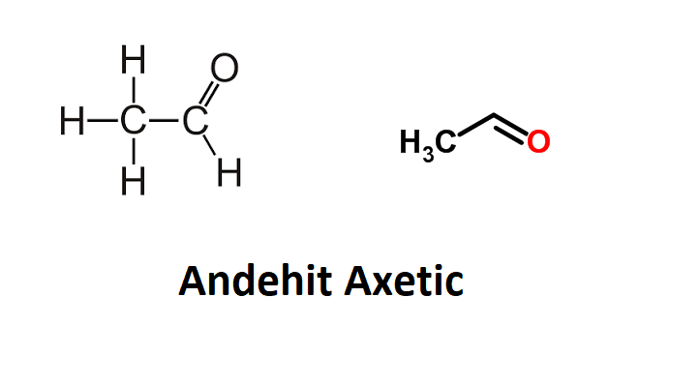
Y là acetaldehyde (CH3CHO), một hợp chất có giá trị trong nhiều ứng dụng hóa học.
Dưới đây là mô tả chi tiết về các phản ứng:
- Đầu tiên, glucose (C6H12O6), một loại đường tự nhiên phổ biến trong thực phẩm, trải qua chuỗi phản ứng để tạo ra các sản phẩm cuối cùng.
- Trong phản ứng đầu tiên, glucose được chuyển hóa thành hai phân tử etanol (C2H5OH) và hai phân tử khí carbon dioxide (CO2).
C6H12O6 → 2C2H5OH + 2CO2
- Tiếp theo, etanol (C2H5OH) phản ứng với oxit đồng (CuO) ở nhiệt độ cao để sản xuất acetaldehyde (CH3CHO), đồng (Cu), và nước (H2O).
CH3CH2OH + CuO → CH3CHO + Cu + H2O
- Cuối cùng, hai phân tử acetaldehyde (CH3CHO) được oxy hóa bởi oxy (O2) ở nhiệt độ cao để tạo ra hai phân tử axit acetic (CH3COOH).
2CH3CHO + O2 → 2CH3COOH
Tổng kết, quá trình chuyển hóa từ glucose thành axit acetic (CH3COOH) trải qua các giai đoạn trung gian etanol và acetaldehyde, và quá trình này có thể ứng dụng trong nhiều lĩnh vực công nghiệp và hóa học.
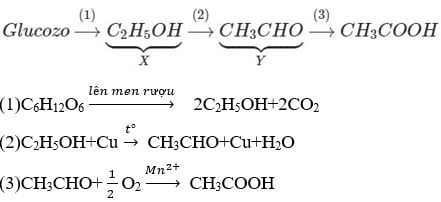
Nguồn: Tổng hợp
2. Đặc điểm vật lý của C2H5OH
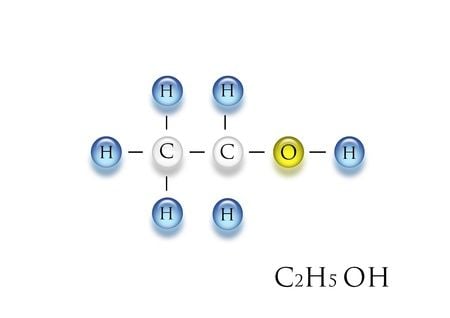
Ancol Etylic, hay còn gọi là Ethanol, rượu etylic, cồn công nghiệp hoặc rượu ngũ cốc, là một hợp chất hữu cơ có vai trò quan trọng trong hóa học và đời sống hàng ngày. Công thức hóa học của ancol etylic là C2H5OH hoặc C2H6O, nhưng đằng sau những ký hiệu đơn giản này là cấu trúc phân tử phức tạp và tính chất hóa học đa dạng.
Cấu trúc phân tử của ancol etylic bao gồm chuỗi nguyên tử cacbon và hydro, với sự kết hợp độc đáo. Nó có một nhóm metyl (CH3-), một nhóm metylen (-CH2-) và một nhóm hydroxyl (-OH). Nhóm metyl là chuỗi hai nguyên tử cacbon liên kết với một nguyên tử hydro, nhóm metylen là một nguyên tử cacbon liên kết với hai nguyên tử hydro, và nhóm hydroxyl là một nguyên tử oxy liên kết với một nguyên tử hydro, tạo thành nhóm -OH có vai trò quan trọng trong nhiều phản ứng hóa học.
Ancol etylic không chỉ là chất gây say, mà còn có nhiều ứng dụng quan trọng trong công nghiệp hóa chất, y học và các lĩnh vực khác. Nó được sử dụng để sản xuất rượu, làm dung môi hóa học, chất khử trùng, và là thành phần chính trong nhiều sản phẩm dược phẩm và mỹ phẩm. Ancol etylic cũng tham gia vào nhiều phản ứng hóa học quan trọng, từ tổng hợp hữu cơ đến sản xuất năng lượng qua quá trình lên men. Với sự kết hợp của các nhóm chức năng và tính chất đa dạng, ancol etylic là một trong những hợp chất hữu cơ quan trọng nhất trong hóa học và công nghiệp hiện đại, ảnh hưởng lớn đến nhiều khía cạnh của cuộc sống.
Đặc điểm vật lý của Ancol Etylic:
- Dạng và Màu sắc: Ancol etylic là một chất lỏng trong suốt không màu, với mùi thơm đặc trưng. Sự trong suốt và mùi thơm này làm cho nó phù hợp cho nhiều ứng dụng khác nhau.
- Tính Bay hơi và Cháy: Ancol etylic rất dễ bay hơi và nhanh chóng chuyển hóa thành dạng khí khi tiếp xúc với không khí. Nó cũng dễ bắt lửa, nên cần thận trọng khi sử dụng.
- Tính Tan trong Nước: Ancol etylic hòa tan hoàn toàn trong nước, không hình thành lớp phân tách. Tính chất này làm cho nó là một dung môi quan trọng trong nhiều quá trình hóa học và ứng dụng sinh học.
- Khối Lượng Riêng: Ancol etylic có khối lượng riêng khoảng 0,7936 g/m3 ở 15°C, và giá trị này có thể thay đổi theo nhiệt độ và áp suất.
- Nhiệt Độ Sôi: Ancol etylic có nhiệt độ sôi là 78,39°C, cho phép nó dễ dàng chuyển từ dạng lỏng sang dạng hơi khi nhiệt độ tăng.
- Hóa Rắn: Ancol etylic trở thành rắn ở nhiệt độ rất thấp, khoảng -114,15°C, trạng thái này thường được sử dụng trong các ứng dụng đông lạnh và làm lạnh công nghiệp.
Các đặc điểm vật lý độc đáo của ancol etylic đã dẫn đến nhiều ứng dụng trong hóa học, công nghiệp, y học và các lĩnh vực khác, khiến nó trở thành một hợp chất quan trọng trong đời sống hàng ngày.
Nguồn: Tổng hợp
3. Những thông tin quan trọng về CH3CHO
CH3COOH, hay còn gọi là axit axetic, là một hợp chất hữu cơ quan trọng và đa năng trong nhiều lĩnh vực. Axit axetic, với công thức hóa học CH3COOH, là một trong những axit hữu cơ mạnh và phổ biến nhất. Từ thời kỳ đồ đá, axit này đã có ảnh hưởng lớn trong ngành công nghiệp, sản xuất thực phẩm và y học. Nó còn được biết đến với nhiều tên gọi khác như etanoic, Hydro axetat (HAc), Ethylic acid, axit metanecarboxylic, dấm, acetic acid, Acid ethanoic, v.v., phản ánh sự quan trọng và đa dạng của nó trong nhiều lĩnh vực.
Axit axetic có nhiều ứng dụng phong phú. Trong công nghiệp, nó được dùng để sản xuất hợp chất hữu cơ và vô cơ, làm dung môi, và chế tạo các sản phẩm như sợi polyester. Trong thực phẩm, nó là thành phần chính của giấm và quan trọng trong quá trình ủ chua. Trong y học, axit axetic được dùng để chuẩn bị dung dịch y tế và thuốc. Nó cũng có vai trò trong các phản ứng tổng hợp hữu cơ và nhiều ứng dụng khác, chứng tỏ sự quan trọng không thể thiếu của nó trong đời sống và ngành công nghiệp toàn cầu.
Khám phá các tính chất vật lý nổi bật của axit này:
- Tính chất vật lý đặc biệt: Axit này xuất hiện dưới dạng lỏng, không màu và có vị chua đặc trưng. Sự không màu và vị chua làm cho nó trở thành một hợp chất quan trọng trong nhiều ứng dụng nhờ vào đặc tính đặc biệt này.
- Nhiệt độ sôi và Nhiệt độ nóng chảy: Axit này có nhiệt độ sôi khoảng 118°C và nhiệt độ nóng chảy khoảng 16,7°C. Điều này cho phép nó dễ dàng chuyển từ dạng lỏng sang dạng hơi khi tăng nhiệt độ, còn ở nhiệt độ phòng, nó vẫn ở dạng lỏng.
- Tính dễ bay hơi: Axit này thuộc nhóm hợp chất dễ bay hơi, tức là nó có khả năng chuyển đổi từ dạng lỏng sang dạng hơi ở nhiệt độ phòng. Điều này làm cho nó thường xuất hiện trong không khí và có thể góp phần vào ô nhiễm không khí.
- Trọng lượng riêng: Trọng lượng riêng của axit này có thể thay đổi theo nhiệt độ và áp suất. Ở 25°C, trọng lượng riêng của nó khoảng 1,049 g/mL, điều này thuận lợi cho nghiên cứu và ứng dụng trong phòng thí nghiệm. Tuy nhiên, trọng lượng riêng có thể thay đổi tùy thuộc vào điều kiện môi trường.
- Hơi áp suất: Hơi áp suất của axit này khoảng 1,5 kPa ở 20°C. Hơi áp suất là yếu tố quan trọng trong quá trình bay hơi và tương tác với các chất khác. Sự thay đổi của hơi áp suất theo nhiệt độ có thể ảnh hưởng đến tính chất của axit axetic trong các ứng dụng thực tế.
Những đặc điểm vật lý này khiến axit này có ứng dụng rộng rãi từ công nghiệp đến nghiên cứu khoa học và các ứng dụng hàng ngày.
Nguồn: Tài liệu sưu tầm
Ngoài ra, có thể tham khảo: Phản ứng hóa học : S + H2SO4 → SO2 + H2O. Cảm ơn bạn.
