Các công thức tính số mol trong hóa học, áp dụng trong các điều kiện chuẩn về thể tích, khối lượng và một số yếu tố khác, là những bài tập phổ biến trong chương trình hóa học lớp 8. Những công thức này đóng vai trò quan trọng trong các bài học hóa học sau này. Nếu bạn muốn ôn lại hoặc tìm hiểu thêm, hãy tham khảo nội dung dưới đây.
Khái niệm về mol và số mol
Để học tốt môn hóa và giải quyết được bài tập phản ứng hóa học, bạn cần hiểu rõ định nghĩa về mol và số mol. Đây là kiến thức cơ bản đầu tiên trong chương trình hóa học lớp 8. Hãy cùng Mytour ôn lại khái niệm này nhé:
Mol là gì?
Theo sách giáo khoa Hóa học lớp 8, trang 63, định nghĩa mol là lượng chất chứa 6.02x10^23 nguyên tử hoặc phân tử của chất đó. Con số 6.02x10^23 này được gọi là số Avogadro.

Khi nghiên cứu một phản ứng hóa học, chúng ta cần xác định số lượng nguyên tử và phân tử của các chất tham gia trong phương trình. Tuy nhiên, việc đếm nguyên tử và phân tử là rất khó, vì vậy các nhà hóa học đã đưa ra khái niệm về mol.
Số mol là gì?
Số mol, ký hiệu là n, là đại diện cho lượng chất. Khi biết số mol của một chất, ta có thể tính được số nguyên tử hoặc phân tử của nó. Trong phản ứng hóa học, các chất phản ứng với nhau theo tỷ lệ của nguyên tử hoặc phân tử. Vì vậy, số mol giúp ta tính chính xác lượng chất tham gia vào phương trình phản ứng, hỗ trợ việc điều chế dung dịch.
Công thức chi tiết tính số mol
Để tính số mol, có thể dựa vào thể tích, khối lượng hoặc các yếu tố khác. Tùy thuộc vào bài tập, khi biết đại lượng nào thì bạn sử dụng công thức tương ứng để tính số mol. Dưới đây là các công thức tính số mol trong hóa học ở điều kiện chuẩn với thể tích, khối lượng và các yếu tố khác:
Công thức tính số mol qua thể tích
Công thức tính số mol ở điều kiện chuẩn (t = 0°C, P = 1 atm) khi biết thể tích khí là n = V/22,4. Từ công thức này, ta cũng có thể suy ra công thức V = n x 22,4.
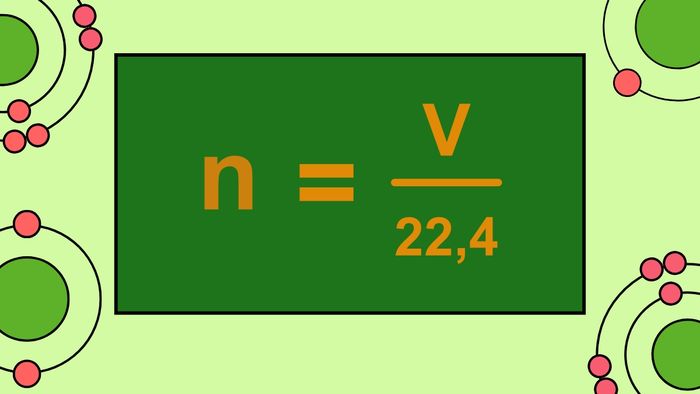
Trong đó:
- V: thể tích khí ở nhiệt độ 0°C và áp suất 1 atm, đơn vị tính là lít. Nếu nhiệt độ và áp suất giữ nguyên, thì 1 mol của tất cả các loại khí đều có thể tích giống nhau.
- n: số mol, đơn vị tính là mol.
Công thức tính số mol qua khối lượng
Để tính số mol khi biết khối lượng, công thức áp dụng cho tất cả các chất rắn, lỏng, khí,... là n = m/M. Từ công thức này, ta có thể tính khối lượng chất tham gia phản ứng nếu biết số mol, m = n.M.
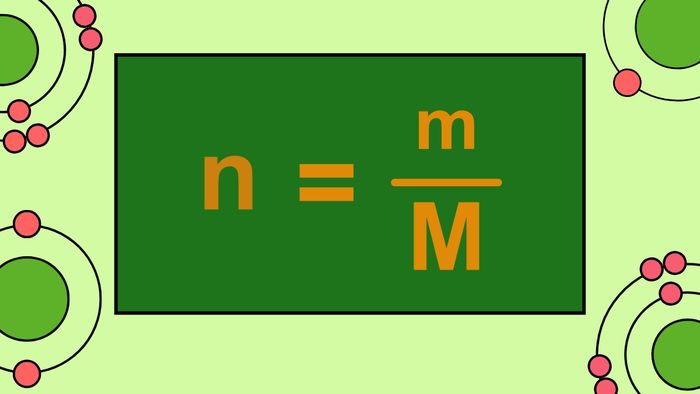
Trong đó:
- m: khối lượng chất, đơn vị tính là gam.
- M: khối lượng mol, đơn vị tính là gam/mol.
Khi tính số mol thông qua khối lượng, bạn cần chú ý một số điểm sau:
- Khối lượng mol của nguyên tử H là 1 gam/mol, vì vậy M của phân tử H2 sẽ là 2 gam/mol.
- Để tính khối lượng mol của hợp chất, bạn thực hiện phép tính cộng và nhân. Ví dụ, phân tử nước H2O có M = 1x2 + 16 = 18 gam/mol.
Các công thức tính số mol khác
Bên cạnh hai công thức đã đề cập, bạn có thể sử dụng một số công thức khác tùy thuộc vào yêu cầu của đề bài và các điều kiện hoặc thông tin có sẵn như sau:
- Nếu biết nồng độ mol C và thể tích chất lỏng V, ta có công thức: n = C.V.
- Nếu biết số nguyên tử hoặc phân tử A: n = A/N (A là số nguyên tử hoặc phân tử, N là hằng số Avogadro).
- Nếu biết áp suất P, thể tích V và nhiệt độ T, công thức tính số mol là: n = (P.V)/(R.T), trong đó R = 0,082.

Để giải các bài tập hóa học, ngoài việc sử dụng máy tính cầm tay, bạn cũng có thể tận dụng điện thoại. Nếu bạn đang tìm mua một chiếc điện thoại, hãy tham khảo thông tin dưới đây:
Một số bài tập ứng dụng công thức tính số mol (kèm lời giải)
Để các học sinh dễ dàng hiểu các dạng bài tập tính số mol, Mytour sẽ cung cấp một số bài tập mẫu kèm lời giải chi tiết dưới đây:

Bài 1: Dựa trên các dữ kiện dưới đây, hãy tính số mol tương ứng:
- a, 11,2 g Fe
- b, 200 ml NaOH 1M
- c, 2,24 ml dung dịch NaCl ở điều kiện chuẩn
Bài giải:
- a, nFe = n/M = 11,2/56 = 0,2 (mol).
- b, nNaOH = C.V = 1 x 0,2 = 0,2 (mol).
- c, nNaCl = V/22,4 = 2,24/22,4 = 0,1 (mol).
Bài 2: Cho 300 gam dung dịch FeCl2 12,7%, tính số mol FeCl2.
Bài giải:
- Khối lượng FeCl2 tính được là: m = (mxC%)/100% = 300x12,7%/100% = 38,1 gam.
- Số mol FeCl2 sẽ là: n = m/M = 38,1/127 = 0,3 mol.
Bài 3: Tính số mol có trong 9.10^23 nguyên tử oxi.
Bài giải:
- Số mol có trong 9.10^23 nguyên tử oxi là: n = A/N = 9.10^23/6,02.10^23 = 1,495 mol.
Trên đây là các công thức tính số mol trong hóa học ở điều kiện chuẩn, áp dụng cho thể tích, khối lượng và một số yếu tố khác. Đây là những bài toán cơ bản trong môn hóa học, nhưng bạn cần ghi nhớ và luyện tập thật kỹ vì chúng sẽ giúp ích cho bạn trong tương lai. Nếu bạn muốn khám phá thêm các công thức của các môn học khác, đừng quên theo dõi những bài viết tiếp theo của Mytour nhé.
